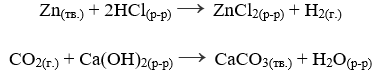Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
- Соединения
- Разложения
- Замещения
- Обмена
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно
сложное вещество. Примеры:
4Na + O2 = 2Na2O
P2O5 + 3H2O = 2H3PO4
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
2KMnO4 = K2MnO4 + MnO2 + 2O2
Сa(OH)2 = CaO + H2O
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
CuSO4 + Fe = FeSO4 + Cu
2KI + Cl2 = 2KCl + I2
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами.
Часто обмен происходит анионами/катионами:
2KOH + MgCl2 = Mg(OH)2↓ + 2KCl
AgF + NaCl = AgCl↓ + NaF
Реакция нейтрализации — реакция обмена между основанием и кислотой, в ходе которой получаются соль и вода:
KOH + H2SO4 = K2SO4 + H2O

Окислительно-восстановительные реакции (ОВР)
Это те химические реакции, в процессе которых происходит изменение степеней окисления химических элементов, входящих в состав
исходных веществ. ОВР подразделяются на:
- Межмолекулярные — атомы окислителя и восстановителя входят в состав разных молекул. Примеры:
- Внутримолекулярные — атомы окислителя и восстановителя в составе одного сложного вещества. Примеры:
- Диспропорционирование — один и тот же атом является и окислителем, и восстановителем
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
K2SO3 + K2Cr2O7 + H2SO4 → K2SO4
+ Cr2(SO4)3 + H2O
KMnO4 → K2MnO4 + MnO2 + O2
KClO3 → KCl + O2
KOH + Cl2 → (t) KCl + KClO3 + H2O
KOH + Cl2 → KCl + KClO + H2O

Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО,
принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
От обилия информации можно запутаться. Я рекомендую сформулировать четко: «Окислитель — понижает СО, восстановитель — повышает СО». Запомнив
эту информацию таким образом, вы не будете путаться.

ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Обратимые реакции — такие химические реакции, которые протекают одновременно в двух противоположных направлениях: прямом и обратном.
При записи реакции в таких случаях вместо знака «=» ставят знак обратимости «⇆».
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
N2 + 3H2 ⇆ 2NH3
CH3COOH + C2H5OH ⇆ CH3COOC2H5 + H2O
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от
обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Иногда сложно бывает отличить обратимую реакцию от необратимой, однако я дам несколько советов, которые советую взять на вооружение.
В результате необратимых реакций:
- Образуются малодиссоциирующие вещества (например — вода, однако есть исключения — реакция этерификации)
- Реакция сопровождается выделение большого количества тепла
- В ходе реакции образуется газ или выпадает осадок
Примеры необратимых реакций:
BaCl2 + H2SO4 = BaSO4↓ + 2HCl (выпадает осадок)
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)

Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому
составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой,
твердой и газообразной.
Все реакции можно разделить на гетеро- и гомогенные. Гетерогенные реакции (греч. heterogenes — разнородный) — реакции, протекающие на
границе раздела фаз, в неоднородной среде. Скорость таких реакций зависит от площади соприкосновения реагирующих веществ.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество,
твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
Zn(тв.) + 2HCl(р-р.) = ZnCl2(р-р.) + H2(газ.)↑

Гомогенные реакции (греч. homogenes — однородный) — реакции, протекающие между веществами, находящимися в одной фазе.
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером
такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
NaOH(р-р.) + CH3COOH(р-р.) = CH3COONa(р-р.) + H2O(р-р.)

Реакции и их тепловой эффект
Все реакции можно разделить на те, в ходе которых тепло поглощается, или, наоборот, тепло выделяется. Представьте пробирку, охлаждающуюся
или нагревающуюся в вашей руке — это и есть тот самый тепловой эффект. Иногда тепла выделяется так много, что реакции сопровождаются
воспламенением или взрывом (натрий с водой).
- Экзотермические реакции
- Эндотермические реакции
Экзотермические реакции (греч. exo — вне) — химические реакции, сопровождающиеся потерей энергии системой и выделением тепла (той самой
энергии) во внешнюю среду. При написании химических реакций в конце экзотермических ставят «+ Q» (Q — тепло), иногда бывает указано точное
количество выделяющегося тепла. Например:
2Mg + O2 = 2MgO + Q
Большинство реакций нейтрализации относятся к экзотермическим:
NaOH + HCl = NaCl + H2O + 56 кДж

К экзотермическим реакциям часто относятся реакции горения, соединения.
4NH3 + 5O2 = 4NO + 6H2O + Q
Исключением является взаимодействие азота и кислорода, при
котором тепло поглощается:
N2 + O2 ⇄ 2NO — Q
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому
не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания»
в реакции вместо явного +Q при экзотермической реакции могут написать ΔH < 0. Например:
2Na + 2H2O = 2NaOH + H2; ΔH < 0 (это значит, что тепло выделяется — реакция экзотермическая)

Эндотермические реакции (греч. ἔνδον — внутри) — химические реакции, сопровождающиеся поглощением тепла, в результате которых образуются
вещества с более высоким энергетическим уровнем (их внутренняя энергия увеличивается).
К таким реакциям наиболее часто относятся реакции разложения. При написании эндотермических реакций в конце ставят «-Q», либо указывают точное
количество поглощенной энергии. Примеры таких реакций:
2HgO = Hg + O2 — Q
CaCO3 = CaO + CO2↑ — Q
С целью «запутывания» может быть дана энтальпия, она при таких реакциях всегда: ΔH > 0, так как внутренняя
энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)

Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик»)
является примером экзотермического разложения, при котором тепло выделяется.

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
1.4.1. Классификация химических реакций в неорганической и органической химии.
Классификация химических реакций на основании их признаков.
Классификационный признак |
Тип реакции |
Число и состав реагентов и продуктов |
соединенияв результате таких реакций из двух или более исходных веществ образуется только один продукт, например: С + O2 = CO2 4NO2 + O2 + 2H2O = 4HNO3 |
разложенияв таких реакциях из одного вещества образуется два или больше других веществ: 2KMnO4 = K2MnO4 + MnO2 + O2 CaCO3 = CaO + CO2 |
|
замещенияВсе реакции, в результате которых из простого и сложного веществ образуется другое простое и другое сложное вещества. Например: Zn + CuSO4 = ZnSO4 + Cu
|
|
обменаРеакциями обмена называют такие реакции, в результате которых вещества меняются своими составными частями. Например: 2NaOH + CuCl2 = 2NaCl + Cu(OH)2 Частный случай реакции обмена между кислотой и основанием носит также название реакции нейтрализации: NaOH + HCl = NaCl + H2O
|
|
Изменение степеней окисления химических элементов |
окислительно-восстановительныев результате таких реакций изменяются степени окисления одного или более химических элемента. Например: |
Реакции, протекающие с сохранением степеней окисления атомов всех химических элементов |
|
Обратимость |
обратимыетакие реакции обладают способностью протекать как в прямом, так и обратном направлении. Реакции, про которые обязательно нужно знать, что они обратимые: |
необратимыеТакие реакции протекают только в прямом направлении. Если речь идет о реакциях между электролитами, то необратимой реакция является в том случае, если образуется осадок, газ или малодиссоциирующее вещество. Например: Na2CO3 + 2HCl = 2NaCl + H2O + CO2 В качестве малодиссоциирующих веществ в реакциях ионного обмена могут образоваться вода, слабые кислоты, гидроксид аммония. |
|
Тепловой эффект |
экзотермическиеВ результате таких реакций выделяется энергия в виде теплоты. Обозначают такие реакции, добавляя «+Q» к уравнению реакции, например: |
эндотермическиеПри протекании таких реакций поглощается тепло. Для обозначения таких реакций пишут «-Q» в уравнении реакции. Практически все реакции разложения являются эндотермическими: Исключения: реакции разложения HI и NO являются экзотермическими. |
|
Количество фаз |
гомогенныеГомогенными реакциями называют такие реакции, реагенты в которых находятся в одной фазе. Примерами таких реакций могут быть многие реакции протекающие в растворах, реакции между газообразными веществами: NaOH (р-р) + HCl(р-р) = NaCl + H2O 2CO + O2 = 2CO2 В гомогенных реакциях не наблюдаются границы раздела между реагентами |
гетерогенныегетерогенными реакциями называют такие реакции, в которых реагирующие вещества находятся в разных фазах. Примерами таких реакций являются, взаимодействие цинка с раствором соляной кислоты, взаимодействие углекислого газа с известковой водой, и т.д.: |
|
По участию катализатора |
каталитическиереакции, протекающие в присутствии катализатора:
|
некаталитическиереакции, протекающие без катализатора: |
Классификация химических реакций в органической химии:
Реакции присоединения |
В зависимости от того, какое соединение присоединяется органическим веществом различают:
Гидрирование — присоединение водорода:Гидратация — присоединение воды:Гидрогалогенирование — присоединение галогеноводорода:
|
Реакции замещения |
Под реакциями замещения в органической химии подразумевают такие реакции, в результате протекания которых происходит замена одного заместителя (или атома водорода) непосредственно прикрепленного к углеродному скелету на другой заместитель. Так, например, реакциями замещения являются: Галогенирование алканов:Нитрование углеводородов:Реакция спиртов с галогеноводородными кислотами:C2H5OH + HBr = C2H5Br + H2O и т.д. |
Реакции отщепления (элиминирования) |
Все реакции, в названии которых присутствует приставка «де-«: дегидрирование:дегидратация:дегидрогалогенирование:(от исходной молекулы бромэтана отщепляется бромоводород, который нейтрализуется щелочью) дегалогенирование:Также к реакциям отщепления (элиминирования) относят крекинг — процесс термического превращения углеводородов в соединения с меньшей длинной углеродного скелета. Например, крекинг алканов, уравнение которого в общем виде можно записать как: |
Окислительно-восстановительные реакции |
Реакции, при которых изменяется степень окисления одного или нескольких атомов углерода углеродного скелета. Окисление органического соединенияВ таких реакциях отдельные атомы углерода повышают свою степень окисления. Например: Восстановление органического соединенияЧаще всего под восстановлением органических веществ понимают их взаимодействие с водородом. Например: CH3-CH=O + H2 => CH3-CH2-OH |
Реакции с сохранением качественного и количественного состава веществ |
Изомеризация |
Реакции протекающие по тем или иным механизмам |
Реакции протекающие по ионному механизмуВ таких реакциях активными действующими частицами являются ионы. Следует помнить, что по ионному механизму протекают такие реакции как:
|
Реакции протекающие по радикальному механизмуВ таких реакциях активными действующими частицами являются свободные радикалы:
|
Тема 2. СТРОЕНИЕ АТОМА.
Атом – мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Электронная оболочка – совокупность движущихся вокруг ядра электронов.
Атомное ядро – центральная, положительно заряженная, часть атома, состоящая из протонов и нейтронов, связанных между собой ядерными силами.
|
Протон р+ |
Нейтрон n0 |
Электрон е |
|
|
Заряд частицы |
+1 |
0 |
-1 |
|
Масса частицы |
1,00728 а.е.м. |
1,00866 а.е.м. |
1/1840 от массы протона |
Заряд ядра атома Z равен порядковому номеру элемента в периодической системе.
Химический элемент – вид атомов, с определённым зарядом ядра.
Так как атом – электронейтрален (не заряжен), то число протонов в атоме равно числу электронов (число + = числу — ): N(e—) = N(p) = Z
Массовое число атома А складывается из числа протонов и нейтронов в ядре данного изотопа. Число нейтронов можно найти, вычитая заряд ядра атома из массового числа. А = N(p) + N(n) N(n) = A – Z
Oдин и тот же химический элемент может существовать в виде двух или нескольких изотопов.
Изотопы – атомы с одинаковым зарядом ядра, но разным массовым числом, т.е разным числом нейтронов в ядре.
Нейтроны практически не влияют на химические свойства элементов, все изотопы одного и того же элемента химически неотличимы.
Пример 1: Определить число нейтронов у изотопов углерода: 12С и 14С.
Решение: у 12С – 6 нейтронов (12-6=6), у 14С – 8 нейтронов (14-6=8).
Пример 2: определить число протонов и нейтронов в ядре изотопа мышьяка с массовым числом 75.
Решение: порядковый номер у As – 33. Следовательно, заряд ядра Z= +33, число протонов – 33. Число нейтронов: A – Z = 75 – 33 = 42.
ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА.
В 1913 г датский физик Н. Бор предложил модель атома, в которой электроны вращаются вокруг ядра атома, как планеты обращаются вокруг Солнца.
|
|
Бор предположил, что электроны в атоме могут устойчиво существовать только на орбитах, удаленных от ядра на строго определенные расстояния. Эти орбиты он назвал стационарными. Электронные орбиты в модели Бора обозначаются целыми числами: 1, 2, …, n, начиная от ближайшей к ядру. |
Такие орбиты называют электронными уровнями (слоями).
Уровни состоят из близких по энергии подуровней (электронных оболочек).
Их обозначают s, p, d, f.
Подуровни состоят из одинаковых по энергии орбиталей.
На каждой орбитали может быть не больше двух электронов.
Они отличаются так называемым СПИНОМ, упрощенно – направлением вращения.
Принцип Паули (запрет Паули) ограничивает число электронов, которые могут находиться на одной орбитали.
Согласно принципу Паули, на любой орбитали может находиться не более двух электронов и лишь если они имеют противоположные спины.
Правило Хунда определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию. Оно было выведено немецким физиком-теоретиком Ф. Хундом в 1927 г. на основе анализа атомных спектров.
Согласно правилу Хунда, заполнение орбиталей одного и того же подуровня происходит таким образом: сначала каждую орбиталь занимают по одному электрону, а затем уже по второму, с противоположным спином.
Пример: атом азота имеет три электрона, находящиеся на 2р-подуровне. Согласно правилу Хунда, они должны располагаться поодиночке на каждой из трех 2р-орбиталей. При этом все три электрона должны иметь параллельные спины:
Связь между уровнем и подуровнями.
|
Номер электронного слоя (уровня) |
Электронные подуровни |
Максимальное число электронов |
|
n = 1 |
1s ◻ |
2e |
|
n = 2 |
2s ◻ 2p ◻◻◻ |
2e 6e |
|
n = 3 |
3s ◻ 3p ◻◻◻ 3d ◻◻◻◻◻ |
2e 6e 10e |
|
n = 4 |
4s ◻ 4p ◻◻◻ 4d ◻◻◻◻◻ 4f ◻◻◻◻◻◻◻ |
2e 6e 10e 14e |
ЭЛЕКТРОННЫЕ КОНФИГУРАЦИИ АТОМОВ
Изображение орбиталей с учетом их энергии называется энергетической диаграммой атома.
На каждом s-подуровне (одна орбиталь) могут находиться два электрона, на каждом p-подуровне (три орбитали) — шесть электронов, на каждом d-подуровне (пять орбиталей) — десять электронов.
Принцип минимума энергии определяет порядок заселения атомных орбиталей, имеющих различные энергии. Согласно принципу минимума энергии, электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.
Энергия подуровней растет в ряду:
1s < 2s < 2 p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f∼5d < 6p < 7s <5f∼6d…
Оказалось, что у одних элементов более низкую энергию имеет 4f-подуровень, а у других — 5d-подуровень.
То же самое наблюдается для 5f- и 6d-подуровней.
ПОСЛЕДОВАТЕЛЬНОСТЬ ЗАПОЛНЕНИЯ ОРБИТАЛЕЙ У ПЕРВЫХ 36 АТОМОВ.
Электронная формула атома – запись распределения электронов по орбиталям в основном (невозбужденном) состоянии атома или его ионов: 1s22s22p63s23p6… и т.д.
Заполнение электронных оболочек атомов первых 4-х периодов.
Водород (1е): Н 1s1 – заполняется первый уровень.
Гелий (2е) Не 1s2
ПЕРВЫЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ ЗАПОЛНЕН.
Литий (3е) — начинает заполняться второй уровень: Li 1s22s1
Бериллий на 2s-подуровень приходит второй электрон.
Затем у бора начинается заполнение 2p-подуровня:
В 1s22s22p1
У следующих за бором пяти атомов продолжается заполнение 2р-подуровня, вплоть до неона: Ne 1s22s22p6
ВТОРОЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ ПОЛНОСТЬЮ ЗАВЕРШЕН.
Начинается третий период – сначала происходит заполнение 3s-подуровня у натрия и магния (это s-элементы), а потом заполняется 3р-подуровень у шести р-элементов: от алюминия до аргона.
Na 1s22s22р63s1 Mg 1s22s22р63s2
Al 1s22s22р63s23p1 ….. Ar 1s22s22р63s23p6
У аргона — инертного газа на внешнем слое 8 электронов.
Распределение электронов по электронным уровням у атома № 18 — аргона выглядит так: 2,8,8.
При этом третий электронный уровень ещё не заполнен: в нём есть 3d-подуровень.
Однако атом № 19 – калий является первым элементом 4 периода, у него идёт заполнение 4s-подуровня.
Калий — это s-элемент.
K 1s22s22p63s23p64s1
3d-подуровень пока остаётся незаполненным.
4s-подуровень заполняется и у кальция: Са 1s22s22p63s23p64s2
И вот ТОЛЬКО у следующих 10 элементов (от скандия до цинка) происходит заполнение 3d-подуровня. Это d-элементы.
Sc 1s22s22p63s23p63d14s2
Ti 1s22s22p63s23p63d24s2
V 1s22s22p63s23p63d34s2
У ванадия на d-подуровне 3 электрона, на 4s — 2 электрона.
Казалось бы, у хрома должно получиться: Сr …3d44s2
Однако у хрома происходит переход одного электрона с s-подуровня на d-подуровень: Сr…3d54s1
Это явление называется ПРОВАЛ ЭЛЕКТРОНА, причина такого явления — более выгодная по энергии полузаполненная d-оболочка.
Дальше у марганца снова происходит «возвращение» электрона на 4s-подуровень: Mn…3d54s2
У атомов с №26 (железо) до № 28 (никель) происходит дальнейшее заполнение 3d-подуровня.
У никеля на d-подуровне 8 электронов, на 4s — 2 электрона. У меди вновь происходит переход одного электрона с s на d-подуровень: Сu …3d104s1
Это снова ПРОВАЛ ЭЛЕКТРОНА, причина которого — более выгодная по энергии полностью заполненная d-оболочка.
И наконец, цинк завершает ряд из 10 d-элементов 4 периода:
Zn 1s22s22p63s23p63d104s2
ТРЕТИЙ ЭЛЕКТРОННЫЙ УРОВЕНЬ только теперь ЗАВЕРШЕН – на нем 18 электронов.
Со следующего элемента 4 периода — галлия вновь начинается заполнение внешнего электронного уровня (№4), теперь уже 4p-подуровня – от галлия до криптона.
Ga 1s22s22p63s23p63d104s24p1 ……… Kr 1s22s22p63s23p63d104s24p6
Для краткости записи электронной конфигурации атома вместо орбиталей, полностью заселенных электронами, иногда записывают символ благородного газа, имеющего соответствующую электронную формулу: 1s2 = [He] 1s22s22p6 = [Ne]
Пример: электронная формула атома хлора 1s22s22p63s23p5, или [Ne]3s23p5.
ЭЛЕКТРОННЫЕ ФОРМУЛЫ ИОНОВ.
Ионы – заряженные частицы; катионы – положительно заряженные ионы, анионы – отрицательно заряженные ионы.
Ионы получаются из атомов путем отдачи электронов (тогда образуются катионы) или принятия электронов (образуются анионы).
S0 (атом серы)+ 2e → S2−(сульфид-анион)
Cu0(атом меди) -2е →Cu2+ (катион меди)
Электронная формула иона получается путём добавления или отнятия электронов в электронной формуле атома.
Электроны сначала уходят с внешнего электронного уровня!
Пример: составить электронные формулы ионов: As3- ; Cu2+.
1) As0 1s22s22p63s23p63d104s24p3 → As3- 1s22s22p63s23p63d104s24p6 (добавились ещё 3 электрона на внешний уровень – их стало 8, а всего – 36е: оболочка инертного газа криптона)
2) Cu01s22s22p63s23p63d104s1 → Cu2+1s22s22p63s23p6 3d9 (уходят 2 электрона, сначала ВНЕШНИЙ 4s-электрон, а потом – 3d-электроны! )
Изоэлектронные частицы – это атомы и ионы, имеющие одинаковое строение электронной оболочки. Например, ион Са2+ и атом аргона – имеют одинаковую 18- электронную оболочку.
Пример: какие из этих солей образованы изоэлектронными ионами: хлорид натрия, фторид бария, бромид магния, сульфид кальция.
NaCl Na+(10e), Cl —(18e), BaF2 Ba2+(54 e), F — (10e);
MgBr2 Mg2+(10e),Br — (36e) CaS Ca2+(18e),S2-(18e)–ионы изоэлектронны. Ответ: CaS
ОСНОВНОЕ И ВОЗБУЖДЕННОЕ СОСТОЯНИЕ АТОМА.
Основное состояние атома — это наиболее выгодное по энергии состояние, которое получается в результате последовательного заполнения оболочек электронами согласно правилу Хунда и принципу минимума энергии.
Поэтому ПРИ НАЛИЧИИ СВОБОДНЫХ ОРБИТАЛЕЙ и при наличии некоторой ЭНЕРГИИ (энергия возбуждения) электроны атома могут РАСПАРИВАТЬСЯ и атом переходит в возбужденное состояние. При этом число неспаренных электронов, а, следовательно, ЧИСЛО СВЯЗЕЙ, образуемых атомом, УВЕЛИЧИВАЕТСЯ.
Пример: у атома углерода на внешнем валентном слое есть 4 электрона. В невозбуждённом (основном) состоянии число неспаренных электронов равно ДВУМ: С … 2s2 2p2
|
↑↓ |
↑ |
↑ |
При переходе одного электрона с s-оболочки на р – оболочку число неспаренных электронов становится равным ЧЕТЫРЁМ: С* …2s12p3
|
↑ |
↑ |
↑ |
↑ |
Это возбужденное состояние углерода.
Тема 3. ПЕРИОДИЧЕСКИЙ ЗАКОН
Д.И. Менделеев в 1869 году так сформулировал Периодический закон: «Свойства элементов, а потому и свойства образуемых ими простых и сложных тел находятся в периодической зависимости от их атомного веса«.
Менделеев учитывал, что для некоторых элементов атомные массы могли быть определены недостаточно точно. После того, как было доказано ядерное строение атома и равенство порядкового номера элемента заряду ядра его атома, Периодический закон получил новую формулировку:
«Свойства элементов, а также образуемых ими веществ находятся в периодической зависимости от заряда их атомных ядер».
Современная Периодическая система состоит из 7 периодов (седьмой период заканчивается 118-м элементом).
Короткопериодный вариант Периодической системы содержит 8 групп элементов, каждая из которых условно подразделяется на группу А (главную) и группу Б (побочную). В длиннопериодном варианте Периодической системы — 18 групп, имеющих те же обозначения, что и в короткопериодном.
В группах, обозначенных буквой А (главных подгруппах), содержатся элементы, в которых идет заселение s- и р-оболочек: s-элементы (IA- и IIA-группы) и р-элементы (IIIA-VIIIA-группы). В группах, обозначенной буквой Б (побочных подгруппах), находятся элементы, в которых заселяются d-подуровни — d-элементы.
Номер периода в Периодической системе соответствует числу энергетических уровней атома данного элемента, заполненных электронами.
Номер периода = Число энергетических уровней, заполненных электронами = номер последнего энергетического уровня
Номер группы в Периодической системе определяет число валентных электронов в атомах s- и p-элементов.
ЗАКОНОМЕРНОСТИ ИЗМЕНЕНИЯ СВОЙСТВ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ.
1) Атомные и ионные радиусы.
Радиус атома – это расстояние от центра ядра до внешнего уровня (области максимальной электронной плотности внешнего уровня).
В периодах орбитальные атомные радиусы по мере увеличения заряда ядра уменьшаются, т.к. растет заряд ядра и => притяжение внешнего электронного уровня к ядру.
В подгруппах радиусы в основном увеличиваются из-за возрастания числа электронных слоёв.
У s- и p-элементов изменение радиусов как в периодах, так и в подгруппах более заметно, чем у d- и f-элементов, поскольку d- и f-электроны находятся на внутренних, а не внешних уровнях.
Уменьшение радиусов у d- и f-элементов в периодах называется d- и f-сжатием.
Образование ионов приводит к изменению ионных радиусов по сравнению с атомными.
Радиусы катионов всегда меньше, а радиусы анионов всегда больше соответствующих атомных радиусов.
Изоэлектронные ионы – это ионы, имеющие одинаковое электронное строение.
Радиус изоэлектронных ионов уменьшается слева направо по периоду, т.к. заряд ядра увеличивается и растёт притяжение внешнего электронного уровня к ядру.
Пример: изоэлектронные ионы с электронной оболочкой, соответствующей аргону – (18 е): S2-, Cl—, K+, Ca2+ и т.п. В этом ряду радиус уменьшается, т.к. растёт заряд ядра.
2) Электроотрицательность— это способность атома элемента к притягивать к себе электроны в химической связи.
Электроны в общей электронной паре смещены к атому того элемента, который имеет большую электроотрицательность.
Слева направо по периоду происходит увеличение электроотрицательности, т.к. растёт заряд ядра и внешний уровень притягивается к ядру сильнее.
Сверху вниз по подгруппе электроотрицательность уменьшается, т.к. увеличивается число электронных уровней и увеличение радиуса. Внешние электроны слабее притягиваются к ядру.
На рис. приведены значения электроотрицательности различных элементов по Полингу.
Металлами являются:
-все элементы побочных подгрупп (d-элементы);
— лантаноиды, актиноиды;
-все s- элементы, кроме водорода и гелия.
р-элементы делятся диагональю на металлы и неметаллы:
|
Ве |
В |
||||
|
Al |
Si |
||||
|
Ge |
As |
неметаллы |
|||
|
металлы |
Sb |
Te |
22 штуки |
||
|
Po |
At |
Каждый период начинается щелочным металлом (или водородом), а заканчивается инертным газом.
3) Валентность – число связей, которые образует атом в молекуле.
Высшая валентность как правило равна номеру группы (исключения – элементы второй половины второго периода – азот, кислород, фтор, инертные газы – гелий, неон, аргон, а также металлы побочных подгрупп первой и VIIIB группы (второй и третий элемент «триады»)).
4) Степень окисления – условный заряд у атома в молекуле, рассчитанный, исходя из предположения, что все связи в молекуле – ионные (т.е. электроны полностью смещены от менее электроотрицательного атома к более электроотрицательному.
Высшая положительная степень окисления определяется числом валентных электронов и равна номеру группы. У s- и р-элементов она равна числу внешних электронов. У d-элементов (кроме групп IB,IIB и VIIIB) — она равна числу d+s электронов.
Исключения: 1) фтор, кислород
2) инертные газы – гелий, неон, аргон.
3) медь, серебро, золото
4) кобальт, никель, родий, палладий, иридий, платина.
Для неметаллов также характерна низшая (отрицательная) степень окисления:
Отрицательная степень окисления неметалла = 8 – номер группы.
5) Высшие оксиды и гидроксиды.
1) Степень окисления элемента в высшем оксиде и гидроксиде равна номеру группы:
SeO3 – высший оксид селена.
2) Чем активнее металл, тем более выражены основные свойства высшего оксида и гидроксида.
3) Чем активнее неметалл и чем больше высшая степень окисления – тем сильнее выражены кислотные свойства.
6) ВОДОРОДНЫЕ СОЕДИНЕНИЯ.
Существует два типа водородных соединений:
- Ионные солеобразные гидриды
Это соединения активных металлов с водородом, в которых водород имеет отрицательную степень окисления: СаН2 – гидрид кальция. Это кристаллические вещества, похожие по виду на соли, поэтому их называют СОЛЕОБРАЗНЫМИ.
- ЛЕТУЧИЕ водородные соединения – их образуют только НЕМЕТАЛЛЫ.
В них отрицательную степень окисления имеет неметалл, а водород имеет степень окисления +1. Все газы, кроме воды.
Особенности свойств летучих водородных соединений.
Темы кодификатора: обратимые и необратимые реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов.
Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» (задание 24 ЕГЭ по химии) ( с ответами)
По возможности протекания обратной реакции химические реакции делят на обратимые и необратимые.
Обратимые химические реакции – это реакции, продукты которых при данных условиях могут взаимодействовать друг с другом.
Например, синтез аммиака — реакция обратимая:
N2 + 3H2 = 2NH3
Процесс протекает при высокой температуре, под давлением и в присутствии катализатора (железо). Такие процессы, как правило, обратимые.
Необратимые реакции – это реакции, продукты которых при данных условиях взаимодействовать друг с другом не могут.
Например, реакции горения или реакции, протекающие со взрывом — чаще всего, необратимые. Горение углерода протекает необратимо:
C + O2 = CO2
Более подробно про классификацию химических реакций можно прочитать здесь.
Вероятность взаимодействия продуктов зависит от условий проведения процесса.
Так, если система открытая, т.е. обменивается с окружающей средой и веществом, и энергией, то химические реакции, в которых, например, образуются газы, будут необратимыми.
Например, при прокаливании твердого гидрокарбоната натрия:
2NaHCO3 → Na2CO3 + CO2↑+ H2O
выделяется газообразный углекислый газ и улетучиватся из зоны проведения реакции. Следовательно, такая реакция будет необратимой при данных условиях.
Если же рассмотреть замкнутую систему, которая не может обмениваться веществом с окружающей средой (например, закрытый ящик, в котором происходит реакция), то углекислый газ не сможет улететь из зоны проведения реакции, и будет взаимодействовать с водой и карбонатом натрия, то реакция будет обратимой при данных условиях:
2NaHCO3 ⇔ Na2CO3 + CO2 + H2O
Рассмотрим обратимые реакции. Пусть обратимая реакция протекает по схеме:
aA + bB ⇔ cC + dD
Скорость прямой реакции по закону действующих масс определяется выражением:
v1=k1·CAa·CBb
Скорость обратной реакции:
v2=k2·CСс·CDd
Здесь k1 и k2 – константы скорости прямой и обратной реакции соответственно, СA, CB, CC, CD – концентрации веществ А, В, С и D соответственно.
Если в начальный момент реакции в системе нет веществ C и D, то сталкиваются и взаимодействуют преимущественно частицы A и B, и протекает преимущественно прямая реакция.
Постепенно концентрация частиц C и D также начнет повышаться, следовательно, скорость обратной реакции будет увеличиваться. В какой-то момент скорость прямой реакции станет равна скорости обратной реакции. Это состояние и называют химическим равновесием.
Таким образом, химическое равновесие — это такое состояние системы, при котором скорости прямой и обратной реакции равны.
Так как скорости прямой и обратной реакции равны, скорость образования реагентов равна скорости их расходования, и текущие концентрации веществ не изменяются. Такие концентрации называют равновесными.
Обратите внимание, при равновесии протекает и прямая, и обратная реакции, то есть реагенты взаимодействуют друг с другом, но и продукты взаимодействуют друг с другом с такой же скоростью. При этом внешние факторы могут воздействовать и смещать химическое равновесие в ту или иную сторону. Поэтому химическое равновесие называют подвижным, или динамическим.
Исследования в области подвижного равновесия начались еще в XIX веке. В трудах Анри Ле-Шателье были заложены основы теории, которые позже обобщил ученый Карл Браун. Принцип подвижного равновесия, или принцип Ле-Шателье-Брауна, гласит:
Если на систему, находящуюся в состоянии равновесия, воздействовать внешним фактором, который изменяет какое-либо из условий равновесия, то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Иными словами: при внешнем воздействии на систему равновесие сместится так, чтобы компенсировать это внешнее воздействие.
Этот принцип, что очень важно, работает для любых равновесных явлений (не только химических реакций). Однако мы сейчас рассмотрим его применительно к химическим взаимодействиям. В случае химических реакций внешнее воздействие приводит к изменению равновесных концентраций веществ.
На химические реакции в состоянии равновесия могут воздействовать три основных фактора – температура, давление и концентрации реагентов или продуктов.
1. Как известно, химические реакции сопровождаются тепловым эффектом. Если прямая реакция идет с выделением теплоты (экзотермическая, или +Q), то обратная — с поглощением теплоты (эндотермическая, или -Q), и наоборот. Если повышать температуру в системе, равновесие сместится так, чтобы это повышение компенсировать. Логично, что при экзотермической реакции повышение температуры компенсировать не получится. Таким образом, при повышении температуры равновесие в системе смещается в сторону поглощения теплоты, т.е. в сторону эндотермических реакций (-Q); при понижении температуры — в сторону экзотермической реакции (+Q).
2. В случае равновесных реакций, когда хотя бы одно из веществ находится в газовой фазе, на равновесие также существенно влияет изменение давления в системе. При повышении давления химическая система пытается компенсировать это воздействие, и увеличивает скорость реакции, в которой количество газообразных веществ уменьшается. При понижении давления система увеличивает скорость реакции, в которой образуется больше молекул газообразных веществ. Таким образом: при увеличении давления равновесие смещается в сторону уменьшения числа молекул газов, при уменьшении давления — в сторону увеличения числа молекул газов.
Обратите внимание! На системы, где число молекул газов-реагентов и продуктов одинаково, давление не оказывает воздействие! Также изменение давления практически не влияет на равновесие в растворах, т.е. на реакции, где газов нет.
3. Также на равновесие в химических системах влияет изменение концентрации реагирующих веществ и продуктов. При повышении концентрации реагентов система пытается их израсходовать, и увеличивает скорость прямой реакции. При понижении концентрации реагентов система пытается их наработать, и увеличивается скорость обратной реакции. При повышении концентрации продуктов система пытается их также израсходовать, и увеличивает скорость обратной реакции. При понижении концентрации продуктов химическая система увеличивает скорость их образования, т.е. скорость прямой реакции.
Если в химической системе увеличивается скорость прямой реакции, мы говорим, что равновесие сместилось вправо, в сторону образования продуктов и расходования реагентов. Если увеличивается скорость обратной реакции, мы говорим, что равновесие сместилось влево, в сторону расходования продуктов и увеличения концентрации реагентов.
Например, в реакции синтеза аммиака:
N2 + 3H2 = 2NH3 + Q
повышение давления приводит к увеличению скорости реакции, в которой образуется меньшее число молекул газов, т.е. прямой реакции (число молекул газов-реагентов равно 4, число молекул газов в продуктах равно 2). При повышении давления равновесие смещается вправо, в сторону продуктов. При повышении температуры равновесие сместится в сторону эндотермической реакции, т.е. влево, в сторону реагентов. Увеличение концентрации азота или водорода сместит равновесие в сторону их расходования, т.е. вправо, в сторону продуктов.
Катализатор не влияет на равновесие, т.к. ускоряет и прямую, и обратную реакции.
Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» (задание 24 ЕГЭ по химии) ( с ответами)
166
Создан на
16 января, 2022 От Admin
Химическое равновесие
Тренажер задания 22 ЕГЭ по химии
1 / 10
Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при понижении давления: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) С2Н2(г) + Н2(г) ↔ С2Н4(г) Б) АlСl3(р-р) + Н2О(ж) ↔ Аl(ОН)Сl2(р-р) + НСl(р-р) В) С4Н8(г) + Н2О(г) ↔ С4Н9ОН(г) Г) 2SO2(г) + O2(г) ↔ 2SO3(г) |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
2 / 10
Установите соответствие между уравнением обратимой реакции и направлением смещения химического равновесия при понижении температуры в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) NО(г) + NО2(г) ↔ N2O3(г) + Q Б) С4Н10(г) ↔ С4Н6(г) + 2Н2(г) — Q В) НF(р-р) = Н+(р-р) + F−(р-р) — Q Г) ClF(г) + F2(г) ↔ ClF3(г) + Q |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
3 / 10
Установите соответствие между способом воздействия на равновесную систему
СОСl2(г) ↔ CO(г) + Сl2(г) — Q
и направлением смещения химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) понижение давления Б) добавление катализатора В) увеличение концентрации хлора Г) повышение температуры |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
4 / 10
Установите соответствие между способом воздействия на равновесную систему
[Zn(OH)4]2–(р-р) ↔ Zn2+(р-р) + 4OH–(р-р) – Q
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) увеличение концентрации ионов цинка
Б) добавление кислоты В) пропускание сероводорода Г) добавление твёрдой щёлочи |
1) смещается в сторону прямой реакции
2) смещается в сторону обратной реакции 3) практически не смещается |
5 / 10
Установите соответствие между способом воздействия на равновесную систему:
H2O(ж) + Zn2+(р-р) ↔ ZnOH+(р-р) + H+(р-р) — Q
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) добавление кислоты Б) повышение давления В) добавление твёрдой щёлочи Г) повышение температуры |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
6 / 10
Установите соответствие между фактором, действующим на равновесную систему:
Fe3+(р-р) + 3CNS–(р-р) = Fe(CNS)3 + Q
и направлением смещения химического равновесия в результате этого воздействия.
К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
|
СПОСОБ ВОЗДЕЙСТВИЯ |
НАПРАВЛЕНИЕ СМЕЩЕНИЯ |
|
А) повышение температуры Б) добавление твердого KCNS В) добавление твердого FeCl3 Г) повышение давления |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной 3) практически не смещается |
7 / 10
Установите соответствие между способом воздействия на равновесную систему
СН3СООСН3(ж) + Н2О(ж) ↔ СН3СООН(ж) + СН3ОН(ж) — Q
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) увеличение концентрации спирта Б) добавление катализатора В) отгонка спирта Г) понижение давления |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
8 / 10
Установите соответствие между способом воздействия на равновесную систему
N2(г) + O2(г) ↔ 2NO(г) — Q
и направлением смещения химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) уменьшение концентрации оксида азота(II) Б) увеличение концентрации кислорода В) понижение давления Г) повышение температуры |
1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
9 / 10
Установите соответствие между способом воздействия на равновесную систему
Fe2O3(тв.) + 3H2(г) ↔ 2Fe(тв.) + 3H2О(г)
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой
| ВОЗДЕЙСТВИЕ НА СИСТЕМУ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) повышение давления
Б) добавление катализатора В) увеличение концентрации паров воды Г) уменьшение концентрации водорода |
1) смещается в сторону прямой реакции
2) смещается в сторону обратной реакции 3) практически не смещается |
10 / 10
Установите соответствие между способом воздействия на равновесную систему, в которой протекает реакция
2NH3(г) ⇄ N2(г) + 3Н2(г) – Q
и направлением смещения равновесия при этом воздействии.
К каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СПОСОБ ВОЗДЕЙСТВИЯ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
|
А) увеличение концентрации водорода Б) добавление катализатора В) понижение температуры Г) повышение давления |
1) смещается в направлении прямой реакции 2) смещается в направлении обратной реакции 3) практически не смещается |
Ваша оценка
The average score is 28%
Классификация химических реакций на основании их признаков.
|
Классификационный |
Тип реакции |
|
Число и состав реагентов и |
Соединения — в С + O2 = CO2 NO2 + O2 + H2O |
|
Разложения- в таких 2KMnO4 = K2MnO4 CaCO3 = CaO + CO2 |
|
|
Замещения — Все Zn + CuSO4 = ZnSO4
|
|
|
Обмена — Реакциями 2NaOH + CuCl2 = 2NaCl Частный случай реакции обмена NaOH + HCl = NaCl + H2O
|
|
|
Изменение |
окислительно-восстановительные |
|
Реакции, протекающие |
|
|
Обратимость |
Обратимые — такие |
|
Необратимые — Такие Na2CO3 + В качестве малодиссоциирующих |
|
|
Тепловой |
экзотермические |
|
Эндотермические Исключения: реакции разложения HI |
|
|
Количество |
Гомогенные —Гомогенными NaOH (р-р) + HCl(р-р) = NaCl + H2O 2CO + O2 = 2CO2 В гомогенных реакциях не |
|
Гетерогенные —гетерогенными |
|
|
По |
каталитические реакции, |
|
Некаталитические |
Классификация химических реакций в органической химии:
|
Реакции |
В |
|
Реакции |
Под |
|
Реакции |
Все дегидрирование:
|
|
Окислительно-восстановительные |
Реакции, Окисление В таких Восстановление Чаще всего под восстановлением CH3-CH=O |
|
Реакции с сохранением |
Изомеризация |
|
Реакции |
Реакции В таких реакциях активными
присоединение |
|
Реакции В таких реакциях активными
|