В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол (С6H6) при температуре кипения t = 80 °C. При сообщении бензолу некоторого количества теплоты часть его превращается в пар, который, расширяясь при постоянном давлении, совершает работу, поднимая поршень. Удельная теплота парообразования бензола L = 396·103 Дж/кг, его молярная масса M = 78·10−3 кг/моль. Какая часть подводимого к бензолу количества теплоты идёт на увеличение внутренней энергии системы? Объёмом жидкого бензола и трением между поршнем и цилиндром пренебречь.
Спрятать решение
Решение.
Состояние идеального газа описывается уравнение Менделеева — Клапейрона При кипении масса пара увеличивается, температура пара равна температуре кипения и остаётся постоянной пока весь бензол не выкипит, давление по условию также постоянно. Значит, выполняется соотношение
При передаче газу теплоты Q испаряется бензола. Найдём работу, которую совершает пар:
И по первому началу термодинамики
увеличение внутренней энергии составляет 90,5% от подводимого количества теплоты.
Ответ: 90,5%.
Спрятать критерии
Критерии проверки:
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Приведено полное решение, включающее следующие элементы:
I) записаны положения теории и физические законы, закономерности, применение которых необходимо для решения задачи выбранным способом (в данном случае: уравнение Менделеева—Клапейрона, первый закон термодинамики, выражения для работы газа при изобарном процессе и для внутренней энергии идеального одноатомного газа); II) описаны все вновь вводимые в решении буквенные обозначения физических величин (за исключением обозначений констант, указанных в варианте КИМ, обозначений, используемых в условии задачи, и стандартных обозначений величин, используемых при написании физических законов); III) проведены необходимые математические преобразования и расчёты, приводящие к правильному числовому ответу (допускается решение «по частям» с промежуточными вычислениями); IV) представлен правильный ответ с указанием единиц измерения искомой величины. |
3 |
| Правильно записаны все необходимые положения теории, физические законы, закономерности, и проведены необходимые преобразования. Но имеются один или несколько из следующих недостатков.
Записи, соответствующие пункту II, представлены не в полном объёме или отсутствуют. И (ИЛИ) В решении имеются лишние записи, не входящие в решение (возможно, неверные), которые не отделены от решения (не зачёркнуты; не заключены в скобки, рамку и т. п.). И (ИЛИ) В необходимых математических преобразованиях или вычислениях допущены ошибки, и (или) в математических преобразованиях/вычислениях пропущены логически важные шаги. И (ИЛИ) Отсутствует пункт IV, или в нём допущена ошибка |
2 |
| Представлены записи, соответствующие одному из следующих случаев.
Представлены только положения и формулы, выражающие физические законы, применение которых необходимо для решения данной задачи, без каких-либо преобразований с их использованием, направленных на решение задачи. ИЛИ В решении отсутствует ОДНА из исходных формул, необходимая для решения данной задачи (или утверждение, лежащее в основе решения), но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи. ИЛИ В ОДНОЙ из исходных формул, необходимых для решения данной задачи (или в утверждении, лежащем в основе решения), допущена ошибка, но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи |
1 |
| Все случаи решения, которые не соответствуют вышеуказанным критериям выставления оценок в 1, 2, 3 балла | 0 |
| Максимальный балл | 3 |
Источник: ЕГЭ по физике 2020. Досрочная волна. Вариант 1
Физика ЕГЭ 2021 Демоверсия Решение задания 30
30. В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол (С6H6) при температуре кипения t = 80оC . При сообщении бензолу количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает работу А. Удельная теплота парообразования бензола L = 396 ⋅103 Дж/кг, его молярная масса M = 78 ⋅ 10−3 кг/моль. Какая часть подведённого к бензолу количества теплоты переходит в работу? Объёмом жидкого бензола пренебречь.
Решение:
1. В соответствии с первым законом термодинамики подводимое количество теплоты равно сумме изменения внутренней энергии системы и совершённой механической работы:
При кипении бензола происходит его изобарное расширение. Работа пара
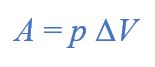
где p – атмосферное давление, Δ V – изменение объёма.
2. Считая пар идеальным газом, воспользуемся уравнением Клапейрона – Менделеева для определения изменения объёма за счёт испарившегося бензола массой
где M = 78⋅10−3 кг/моль – молярная масса бензола, T = 80 + 273 = 353 K – температура кипения бензола.
Отсюда
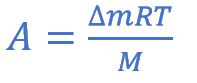
3. Количество теплоты Q, необходимое для испарения массы Δm бензола, пропорционально удельной теплоте парообразования L:
Искомая величина определяется отношением
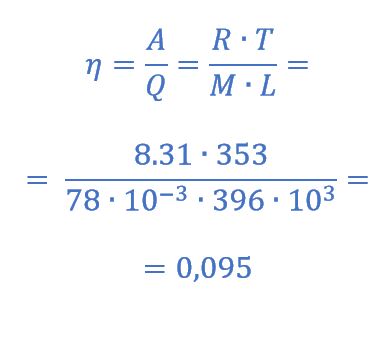
Ответ: 0,095
Похожие записи:
В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол (С6Н6) при температуре кипения t = 80 °C. При сообщении бензолу некоторого количества теплоты часть его превращается в пар, который при изобарном расширении совершает работу, поднимая поршень. Удельная теплота парообразования бензола L = 396 ∙ 103 Дж/кг, а его молярная масса М = 78 • 10-3 кг/моль. Какая часть подводимого к бензолу количества теплоты идёт на увеличение внутренней энергии системы? Объёмом жидкого бензола и трением между поршнем и цилиндром пренебречь.
Обоснуйте применимость используемых законов к решению задачи.
РЕШЕНИЕ
Обоснование
Согласно условию объёмом жидкого бензола следует пренебречь. В то же время возникающие при кипении пары бензола изобарно расширяются, увеличивая свой объём. И это увеличение объёма 
ΔV/N, много больше объёма одной молекулы и поэтому среднее расстояние между соседними молекулами пара много больше их размера. Таким образом, пары бензола в этой задаче являются разреженным газом и их можно описывать моделью идеального газа.
Решение
1. В соответствии с первым началом термодинамики подводимое количество
теплоты равно сумме изменения внутренней энергии системы и совершённой механической работы: 
расширение. Работа пара 

объёма.
2. Считая пар идеальным газом, воспользуемся уравнением Менделеева —
Клапейрона для определения изменения объёма за счёт испарившегося бензола массой 
Т = 80 + 273 = 353 К — температура кипения бензола. Отсюда 
3. Количество теплоты Q, необходимое для испарения массы Δт бензола, пропорционально удельной теплоте парообразования Q = ΔmL.
4. Искомая величина определяется отношением
Ответ: 
Молекулярная физика. Расчетная задача
В. З. Шапиро
Это задание также относится к высокому уровню сложности. Как правило, тематика этого задания «МКТ» и «Термодинамика». Какие-то задачи требуют только формульного решения, какие-то необходимо сопровождать графическими пояснениями термодинамических процессов. В любом случае, теоретический материал полностью соответствует кодификатору элементов содержания и спецификации контрольных измерительных материалов.
1. В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол при температуре кипения
При сообщении бензолу некоторого количества теплоты часть его превращается в пар, который при изобарном расширении совершает работу, поднимая поршень. Удельная теплота парообразования бензола
Дж/кг, а его молярная масса
кг/моль. Какая часть подводимого к бензолу количества теплоты идёт на увеличение внутренней энергии системы? Объёмом жидкого бензола и трением между поршнем и цилиндром пренебречь.
Необходимая теория:
Первый закон термодинамики
Внутренняя энергия
Дано: «СИ»
Дж/кг;
кг/моль.
Найти: — ?
Решение:
Запишем первый закон термодинамики для изобарного процесса:
Выразим из этого равенства изменение внутренней энергии:
Для запишем:
(1).
Работу газа в изобарном процессе можно рассчитать по формуле:
с учетом уравнения Менделеева-Клапейрона получим:
(2).
При совершении работы давление бензола не изменяется, так как поршень в цилиндре легкоподвижный. Давление бензола все время остается равным атмосферному.
При этом
– масса бензола, превратившегося в газообразное состояние.
Количество теплоты, которое идет на превращение бензола в это состояние можно рассчитать по формуле:
Выражение для работы бензола (2) и количества теплоты (3) подставим в уравнение (1).
После сокращения на получим искомую формулу:
Подставим численные значения и проведем расчет:
Ответ: 0,905.
Секрет решения. На первый взгляд задача кажется несложной, но в ней «спрятаны» несколько искусственных приемов, до которых додуматься достаточно сложно. Первый прием – выражение Это математический ход, который сразу подсказывает, что конкретно надо находить в этой задаче.
Второй прием – получение равенства, используя уравнения Менделеева-Клапейрона Здесь надо придерживаться следующих рассуждений: если в левой части уравнения есть переменная величина (в этой задаче
), то и в правой части должна изменяться какая-то физическая величина (в этой задаче
). Можно сказать еще проще: если в левой части равенства есть знак дельта «
«, то и в правой части он должен обязательно появиться. В крайнем случае, можно «перебрать» все величины из правой части: температура не может изменяться, так как при парообразовании она всегда постоянна; молярная масса также неизменна, потому что речь идет об одном и том же газе; R – табличная величина. Остается только
Эти рассуждения помогут понять ситуацию, описанную в задаче и правильно ее решить.
2. Одно и то же постоянное количество одноатомного идеального газа расширяется из одного и того же начального состояния до одного и того же конечного объёма
первый раз по изобаре 1–2, а второй по адиабате 1–3 (см. рисунок). Отношение работы газа в процессе 1–2 к работе газа в процессе 1–3 равно
=к=2. Чему равно отношение х количества теплоты
полученного газом от нагревателя в ходе процесса 1–2, к модулю изменения внутренней энергии газа
в ходе процесса 1–3?
Необходимая теория:
Первый закон термодинамики
Внутренняя энергия
Изопроцессы
Дано:
1–2 р=const;
2–3 Q=const;
=к=2.
Найти:
Решение:
Для участка 1–2 применим первый закон термодинамики с учетом изобарного процесса.
Работу газа при расширении найдем как площадь прямоугольника под графиком.
Изменение внутренней энергии одноатомного идеального газа запишем в виде формулы:
Применим уравнение Менделеева-Клапейрона:
Тогда (3) примет вид:
(4).
Таким образом количество теплоты на участке 12 равно:
(5).
Для участка 1–3 применим первый закон термодинамики с учетом адиабатного процесса.
но так как
запишем:
или
Это выражение означает, что газ на участке 13 совершает работу за счет уменьшения своей внутренней энергии.
Учтем, что по условию =к=2, тогда:
Используя (5) и (6) получим искомую формулу:
Ответ: 5.
Секрет решения. Несмотря на громоздкие расчеты и обилие разных индексов в уравнениях, задача является среднего уровня сложности. Надо знать:
— первый закон термодинамики;
— его применение к изопроцессам;
— формулы, выражающие работу газа и его внутреннюю энергию (только для одноатомного идеального газа);
— уметь «читать» графики;
— понимать, что при расширении газ совершает положительную работу, при сжатии – отрицательную работу;
— проводить рассуждения о том, откуда газ берет энергию для совершения работы (за счет своей внутренней энергии или за счет поступления энергии извне);
— указанные пункты описывать соответствующими уравнениями.
Суть любой задачи по физике – описание физических процессов математическими уравнениями, которые надо решить удобным (рациональным) способом.
3. В тепловом двигателе 1 моль одноатомного разряженного газа совершает цикл 1–2–3–4–1, показанный на графике в координатах p–T, где p – давление газа, Т – абсолютная температура. Температуры в точках 2 и 4 равны и превышают температуру в точке 1 в 2 раза. Определите КПД цикла.
Дано:
Найти: – ?
Решение:
КПД теплового двигателя определяется формулой:
– полезная работа, совершенная газом за цикл, Q – полученное за цикл количество теплоты. Можно графически рассчитать работу, если перерисовать данный цикл в координатах рV. Проведем анализ каждого процесса.
12: V=const, p↑, T↑;
23: p=const, T↑, V↑;
34: V=const, p↓, T↓;
41: p=const, T↓, V↓.
В координатах рV график будет иметь вид:
Работа газа за цикл будет определяться площадью прямоугольника 1-2-3-4.
Учтем, что
Поэтому (на основании закона Шарля).
(на основании закона Гей-Люссака).
Таким образом, можно выразить полезную работу через и
Газ получает положительное количество теплоты на участках 1–2 и 2–3.
Применим к этим участкам первый закон термодинамики.
Но работа газа на этом участке равна нулю, так как процесс изохорный.
С учетом уравнения Менделеева-Клапейрона и
получим:
(2).
Для участка 23 первый закон термодинамики примет вид:
Работа определяется площадью прямоугольника под участком 23.
(4).
С учетом уравнения Менделеева-Клапейрона (4) примет вид:
(5).
Таким образом, полученное количество теплоты на участке 23 равно:
Общее количество теплоты, полученное за цикл:
(6).
Полученные выражения из (1) и (6) подставим в формулу КПД.
Ответ: 15,3%.
Секрет решения. За задачи на определение КПД тепловой машины по графику надо получать максимальные 3 балла. Эти задания сопровождаются большими расчетами, поэтому на первое место надо ставить внимательность их выполнения.
Необходимо выделить следующие моменты в решении:
— определять работу графически можно только в координатах рV;
— если в условии дан график в других координатах, то его надо перечертить в рV;
— поэтапно применять первый закон термодинамики и газовые законы для всех процессов;
— свести в единую формулу полученные данные для расчета КПД.
Спасибо за то, что пользуйтесь нашими материалами.
Информация на странице «Задание 30 ЕГЭ по физике» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ.
Чтобы успешно сдать нужные и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из данного раздела.
Публикация обновлена:
08.03.2023
Обоснование:
Согласно условию объёмом жидкого бензола следует пренебречь. В то же время возникающие при кипении пары бензола изобарно расширяются, увеличивая свой объём. И это увеличение объёма ( Delta V ), судя по условию, заметно. В объёме ( Delta V ) находятся только пары бензола, образовавшиеся при кипении. Следовательно, объём массы пара во много раз больше объёма жидкости, из которой он образовался. Отсюда следует, что объём в паре, приходящийся в среднем на одну молекулу ( Delta V/N ), много больше объёма одной молекулы и поэтому среднее расстояние между соседними молекулами пара много больше их размера. Таким образом, пары бензола в этой задаче являются разреженным газом и их можно описывать моделью идеального газа.
Решение:
1. В соответствии с первым началом термодинамики подводимое количество теплоты равно сумме изменения внутренней энергии системы и совершённой механической работы: ( Q = Delta U + A ). При кипении бензола происходит его изобарное расширение. Работа пара ( A = pDelta V ), где ( p ) — атмосферное давление, ( Delta V ) — изменение объёма.
2. Считая пар идеальным газом, воспользуемся уравнением Менделеева Клапейрона для определения изменения объёма за счёт испарившегося бензола ( Delta m:pDelta V = frac{{Delta m}}{M}RT ), где ( M = 78 cdot {10^{ — 3}} ) кг/моль — молярная масса бензола, ( T = 80 + 273 = 353 ) К — температура кипения бензола. Отсюда ( A = frac{{Delta mRT}}{M} ).
3. Количество теплоты ( Q ), необходимое для испарения массы ( Delta m ) бензола, пропорционально удельной теплоте парообразования ( Q = Delta mL ).
4. Искомая величина определяется отношением
( eta = frac{{Delta U}}{Q} = frac{{Q — A}}{Q} = )( 1 — frac{{RT}}{{ML}} = 1 — frac{{8,31 cdot 353}}{{78 cdot {{10}^{ — 3}} cdot 396 cdot {{10}^3}}} )( approx 0,905 ).
Ответ: ( eta ) ≈ 0,905.
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 
При обращении указывайте id этого вопроса — 15468.
Задание №10322
В вертикальном цилиндре, закрытом лёгким поршнем, находится бензол (С6H6) при температуре кипения t = 80o C. При сообщении бензолу количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает работу А. Удельная теплота парообразования бензола L =396⋅103 Дж/кг, его молярная масса M=78⋅10−3 кг/моль. Какая часть подведённого к бензолу количества теплоты переходит в работу? Объёмом жидкого бензола пренебречь.
Задание состоит в варианте:
Бесплатные вебинары с ответами на все вопросы у нас на канале!
Смотреть
Бесплатные вебинары с ответами на все вопросы у нас на канале!
Смотреть











