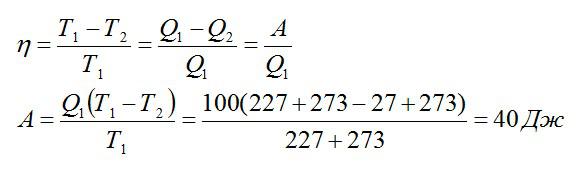в условии
в решении
в тексте к заданию
в атрибутах
Категория:
Атрибут:
Всего: 358 1–20 | 21–40 | 41–60 | 61–80 | 81–100 …
Добавить в вариант
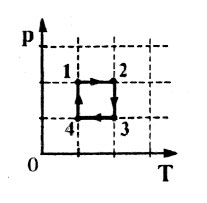
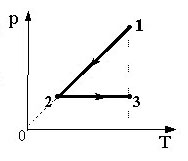
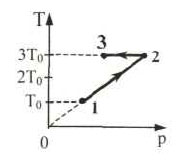
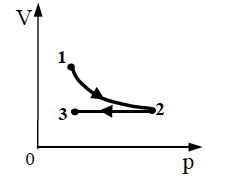
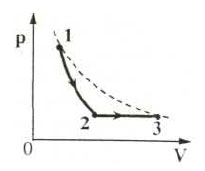
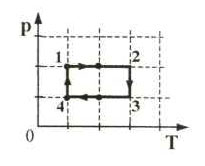
На графиках А и Б приведены диаграммы p−T и p−V для процессов 1−2 и 3−4 (гипербола), проводимых с 1 моль гелия. На диаграммах p – давление, V – объём и T – абсолютная температура газа. Установите соответствие между графиками и утверждениями, характеризующими изображённые на графиках процессы. К каждой позиции первого столбца подберите соответствующую позицию второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами.
ГРАФИКИ
А)
Б)
УТВЕРЖДЕНИЯ
1) Над газом совершают работу, при этом газ отдаёт положительное количество теплоты.
2) Газ получает положительное количество теплоты, при этом его внутренняя энергия не изменяется.
3) Над газом совершают работу, при этом его внутренняя энергия увеличивается.
4) Газ получает положительное количество теплоты, при этом его внутренняя энергия увеличивается.
Источник: ЕГЭ по физике 2017. Досрочная волна. Вариант 101
В цилиндр с подвижным поршнем накачали ν = 4 моля идеального одноатомного газа при температуре t1 = 70 °C. Накачивание вели так, что давление газа было постоянным. Затем накачку прекратили и дали газу в цилиндре расшириться без теплообмена с окружающей средой до давления p = 1 атм. При этом газ остыл до температуры t2 = 30 °C. Какую суммарную работу совершил газ в этих двух процессах? В исходном состоянии цилиндр был пуст и поршень касался дна.
На рисунке показан график зависимости модуля среднеквадратичной скорости Vср.кв. атомов одноатомного идеального газа от объёма V газа в некотором процессе 1→2. Количество атомов газа в течение этого процесса не изменяется.
На основании анализа представленного графика выберите все верные утверждения.
1) В процессе 1→2 газ совершает положительную работу.
2) В процессе 1→2 внутренняя энергия газа уменьшается.
3) В процессе 1→2 давление p газа возрастает прямо пропорционально объёму V газа.
4) В процессе 1→2 газ отдаёт некоторое количество теплоты окружающим телам.
5) Процесс 1→2 является изобарическим.
В вертикальном цилиндре, закрытом лёгким поршнем, находится этиловый спирт при температуре кипения t = 78 °C. При сообщении спирту количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает работу A. Удельная теплота парообразования спирта L = 846 · 103 Дж/кг, а его молярная масса — 46 · 10-3 кг/моль. Какая часть подведённого к этиловому спирту количества теплоты переходит в работу? Объёмом жидкого этилового спирта пренебречь.
Источник: ЕГЭ по физике 13.07.2020. Основная волна. ЦФО. Часть C. Вариант 1
В вертикальном цилиндре, закрытом лёгким поршнем, находится ацетон при температуре кипения t = 56 °C. При сообщении ацетону количества теплоты Q часть его превращается в пар, который при изобарном расширении совершает механическую работу A. Удельная теплота парообразования ацетона L = 524 · 103 Дж/кг, а его молярная масса M = 58 · 10-3 кг/моль. Какая часть подведённого к ацетону количества теплоты идёт на увеличение внутренней энергии системы? Объёмом жидкого ацетона пренебречь.
Источник: ЕГЭ по физике 13.07.2020. Основная волна. ПФО (Самара). Часть C
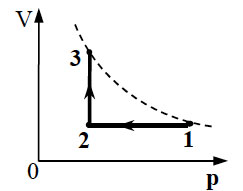
В цилиндрическом сосуде, закрытом подвижным поршнем, находится водяной пар и капля воды. С паром в сосуде при постоянной температуре провели процесс a→b→c, pV−диаграмма которого представлена на рисунке. Из приведённого ниже списка выберите все правильные утверждения относительно проведённого процесса.
1) На участке b→c масса пара уменьшается.
2) На участке a→b к веществу в сосуде подводится положительное количество теплоты.
3) В точке с водяной пар является насыщенным.
4) На участке a→b внутренняя энергия капли уменьшается.
5) На участке b→c внутренняя энергия пара уменьшается.
Источник: Демонстрационная версия ЕГЭ—2021 по физике
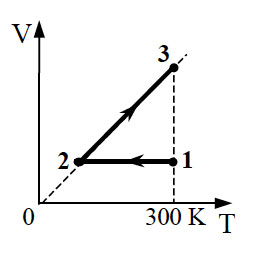
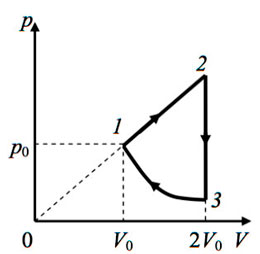
Два моля идеального одноатомного газа совершают циклический процесс, изображённый на диаграмме (см. рис.). Температура газа в состоянии 2 равна 2000 К. Какое количество теплоты получает газ на участке 2−3 этого циклического процесса? Ответ выразите в килоджоулях и округлите до целого числа.
В некотором процессе 1−2 внешние силы совершили над неизменным количеством идеального газа положительную работу 120 Дж. Внутренняя энергия газа в этом процессе изменилась на 100 Дж.
Из приведённого ниже списка выберите все правильные утверждения относительно проведённого процесса.
1) В результате этого процесса газ отдал количество теплоты окружающим телам ().
2) В результате этого процесса температура газа могла только повыситься.
3) Этот процесс представляет собой замкнутый цикл.
4) Объём газа в этом процессе уменьшился.
5) Объём газа в этом процессе увеличился.
Идеальный одноатомный газ занимал объём 4 л при давлении 300 кПа. Затем газ расширился и стал занимать объём 6 л при давлении 150 кПа. В этом процессе газ совершил работу 550 Дж. Какое количество теплоты получил газ в этом процессе, если масса газа в сосуде неизменна?
В ходе адиабатного процесса идеальный одноатомный газ совершил работу 2493 Дж. В результате температура газа понизилась на 50 °C. Найдите количество вещества этого газа. Ответ запишите в молях.
На рисунке показан циклический процесс изменения состояния 1 моль одноатомного идеального газа. На каком участке цикла изменение внутренней энергии газа равно полученному газом количеству теплоты?
Источник: Демонстрационная версия ЕГЭ—2022 по физике
В ходе некоторого процесса температура 1 моля гелия повышается на 200 К.
В этом процессе удельная теплоёмкость гелия постоянна и равна 4991,3 Дж/(кг · °C). Какую работу совершает гелий в этом процессе?
Ответ выразите в Дж и округлите до целого числа.
Идеальный газ получил количество теплоты 300 Дж и совершил работу 100 Дж. Чему равно изменение внутренней энергии газа? Ответ дайте в джоулях.
Идеальный газ получил количество теплоты 300 Дж и при этом внутренняя энергия газа увеличилась на 100 Дж. Какова работа, совершенная газом? (Ответ дать в джоулях.)
Идеальный газ отдал количество теплоты 300 Дж и при этом внутренняя энергия газа увеличилась на 100 Дж. Какова работа, совершенная газом? (Ответ дать в джоулях.)
Идеальный газ отдал количество теплоты 300 Дж и при этом внутренняя энергия газа уменьшилась на 100 Дж. Какова работа, совершенная газом? (Ответ дайте в джоулях.)
Идеальный газ получил количество теплоты 100 Дж и при этом внутренняя энергия газа уменьшилась на 100 Дж. Какова работа, совершенная газом? (Ответ дать в джоулях.)
Если идеальный газ получил количество теплоты 100 Дж, и при этом внутренняя энергия газа увеличилась на 100 Дж, то какую работу совершил газ в этом процессе? (Ответ дайте в джоулях.)
Если идеальный газ отдал количество теплоты 100 Дж и при этом внутренняя энергия газа уменьшилась на 100 Дж, то какова работа, совершенная газом? (Ответ дайте в джоулях.)
Всего: 358 1–20 | 21–40 | 41–60 | 61–80 | 81–100 …
В этой статье рубрики «физика для чайников» рассмотрим подробное решение нескольких задач на работу в термодинамике. Тем, кто хочет научиться решать задачи, рекомендуем систематически тренироваться, предварительно ознакомившись с теорией. А еще, полезно почитать памятку по решению физических задач и держать под рукой основные физические формулы.
Чтобы не заскучать, подписывайтесь на наш телеграм-канал. Там вас ждет ежедневная рассылка, которая будет полезна всем учащимся.
Примеры решения задач на работу в термодинамике
Задача №1. Работа расширения
Условие
При адиабатическом расширении 1 кг воздуха его объем увеличился в 10 раз. Найти работу расширения, если начальное давление 1 атм, а начальная температура 15 °С.
Решение
Зная молярную массу воздуха (29 г/моль), начальный объем можно найти из уравнения Клапейрона-Менделеева:
Не забываем переводить все физические величины из условия в систему СИ.
Из условия находим конечный объем:
Работа равна:
Ответ: 751 кДж.
Задача №2. Работа в цикле Карно
Условие
Температура нагревателя идеальной тепловой машины составляет 227 °С, а охладителя — 27 °С. За один рабочий цикл тепловая машина получает количество теплоты, равное 100Дж. Какую работу совершает рабочее тело идеальной тепловой машины за один цикл?
Решение
Из формулы для КПД можно выразить искомую работу:
Ответ: 40 Дж.
Задача №3. Работа при выдувании мыльного пузыря
Условие
Определить работу, которую необходимо совершить, чтобы выдуть мыльный пузырь диаметром 10 см.
Решение
Работа, которую нужно совершить, чтобы, выдувая мыльный пузырь, увеличить площадь поверхности мыльной пленки на дельта S, равна:
Здесь сигма – коэффициент поверхностного натяжения для мыльного раствора (берется из таблицы). S – общая площадь двух сферических поверхностей пленки мыльного пузыря (внешней и внутренней). S нулевое – площадь этих поверхностей до выдувания пузыря (этой величиной можно пренебречь).
Ответ: 2,5 мДж.
Задача №4. Графическое представление работы
Условие
Газ расширяется от объёма V1 до объёма V2 один раз изотермически, другой изобарно и третий адиабатно. При каком процессе газ совершает большую работу и при каком газу передаётся большее количество теплоты?

Решение
Работа численно равна площади криволинейной трапеции. Из рисунка очевидно, что работа при изобарном процессе будет максимальной, при адиабатном минимальной, т. е.
Ответ: см. выше.
Задача №5. Работа газа
Условие
Газ совершает круговой процесс, состоящий из нескольких этапов. Сначала газ изохорно охлаждается до температуры, при которой его давление равно P2 = 105 Па. Затем он изобарно охлаждается до состояния, из которого возвращается в начальное состояние таким образом, что его давление изменяется с изменением объема по закону Р = αV (α — постоянная величина). Начальные объем и давление газа известны: V1 = 2 м3, Р1 = 4·105 Па. Нарисовать график данного кругового процесса на РV-диаграмме и найти работу, совершенную газом.
Решение
Сначала выполним рисунок:
Точки состояния газа 1 и 3 лежат на прямой, проходящей через центр координат:
C учетом этого, получаем:
Работа газа в данном случае равна площади треугольника 123:
Подставим найденное ранее значение для V3, преобразуем и подставим значения из условия:
Ответ: 2,25*10^5 Дж.
Вопросы на тему «Работа в термодинамике»
Вопрос 1. Что такое работа в термодинамике?
Ответ. Работа – одна из форм обмена энергией термодинамической системы с окружающими телами. Работа, как и энергия, измеряется в Джоулях.
Вопрос 2. Сформулируйте первое начало термодинамики.
Ответ. Первое начало термодинамики гласит:
Изменение внутренней энергии системы равно сумме совершаемой над системой работы внешних сил и количества теплоты, переданной системе.
У первого начала термодинамики исторически есть несколько формулировок. Одна из них: невозможно построить вечный двигатель первого рода.
Вопрос 3. При каком из изопроцессов работа газа равна нулю?
Ответ. При изохорном процессе объем системы остается неизменным. Следовательно, газ в данном процессе не совершает работу.
Вопрос 4. Как, совершая работу, можно изменить внутреннюю энергию?
Ответ. Если работа совершается над телом (системой), то его внутренняя энергия увеличивается, если же тело само совершает работу, это ведет к уменьшению его внутренней энергии.
Вопрос 5. Как определить работу газа геометрически?
Ответ. Величина работы газа равна площади фигуры под графиком на диаграмме pV
Нужна помощь в решении задач или в выполнении других студенческих заданий? Обращайтесь в профессиональный студенческий сервис.
Задачи с графиками: работа газа и внутренняя энергия
Задачи средней сложности, для решения нужна только внимательность. Никаких «подвохов»- все математически четко и понятно.
Задача 1.
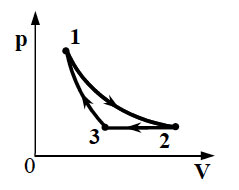
Температура идеального газа в состоянии 1 была . Чему равна температура в состоянии 3 после осуществления процесса 1-2-3, изображенного на диаграмме
?
К.
К задаче 1
Процесс 1-2 – изохорный. Запишем закон Шарля.
Процесс 2-3 – не изотермический, поэтому просто запишем уравнение состояния:
Откуда
Ответ: 1800 К.
Задача 2.
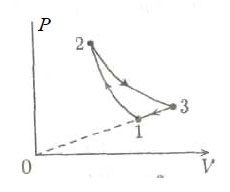
Идеальный одноатомный газ, находящийся при нормальных условиях, переводят из состояния 1 в состояние 2 двумя способами: 1-3-2 и 1-4-2. Найдите отношение количеств теплоты, которые необходимо сообщить 1 кмоль газа в этих двух процессах.
К задаче 2
Рассмотрим переход 1-3-2. Процесс 1-3 – изохора, работа не совершается. Но температура растет, определим, как.
Процесс 3-2 – изобара. Работа в процессе 3-2 равна
Изменение температуры составило . Следовательно, можем определить изменение внутренней энергии:
Теперь найдем общее количество теплоты, переданное газу при таком переходе:
Процесс перехода 1-4-2 отличается только совершенной работой. Определим ее:
Определим отношение количеств теплоты:
Ответ: .
Задача 3.
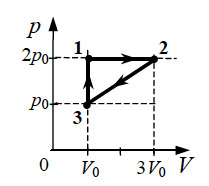
Идеальный одноатомный газ, взятый в количестве 1 моль, переводят из состояния 1 в состояние 4. Какое количество теплоты сообщили в этом процессе газу? Масса газа во время процесса не меняется.
К задаче 3
Определим сначала изменение внутренней энергии, для этого составим объединенный газовый закон для точек 1 и 4.
Изменение внутренней энергии равно
Теперь определим работу. Работу удобно определить как площадь под кривой процесса. Разобьем эту площадь на удобные «куски» — трапеции.
К задаче 3. Определяем работу
Теперь найдем общее количество теплоты, переданное газу:
Ответ: 1450 Дж.
Задача 4.
На рисунке представлена диаграмма цикла с одноатомным идеальным газом, взятым в количестве 0,3 моль. Участки и
— адиабаты. Определите работу, совершенную газом на участке
.
К задаче 4
Участок по условию – адиабата, то есть передачи тепла газу на этом участке не происходит, следовательно, работа будет совершена за счет «внутренних резервов» — то есть внутренней энергии. Нужно, следовательно, найти, как она изменилась.
Задачу можно решить двумя способами. Во-первых, просто определить температуры в точках и
, это легко сделать из данных графика с помощью уравнения Менделеева-Клапейрона, и затем посчитать
. Но, так как
, а
,то изменение внутренней энергии будет равно
Ответ: 1350 Дж.
Задача 5.
Один моль одноатомного идеального газа расширяется сначала изобарно, а затем по линейному закону, причем прямая линия проходит через начало координат .
. Найдите
, если количество тепла, сообщенное газу на участке 1-2, в 4 раза меньше работы, совершенной на участке 2-3.
К задаче 5
Определим количество тепла, сообщенное газу на участке 1-2, и работу, совершенную на участке 2-3.
Для изобарного процесса 1-2 запишем закон Гей-Люссака:
Откуда
Следовательно, изменение внутренней энергии газа равно
Работа на этом участке равна площади под графиком, под участком 1-2:
Тогда тепло, переданное газу, равно
Теперь рассмотрим процесс 2-3. Нам нужно определить лишь работу газа на этом участке. Площадь под этим участком – трапеция, поэтому
Из подобия треугольников и
запишем:
Тогда
Так как по условию , то
Так как , то
Сократим, что возможно:
Из первой записанной нами формулы (закона Гей-Люссака) следует, что
Тогда
Или
Введем замену :
Понятно, отрицательный корень нас не интересует.
Ответ: .
Инфоурок
›
Физика
›Другие методич. материалы›Подборка задач на соответствие «Термодинамика» ЕГЭ
Подборка задач на соответствие «Термодинамика» ЕГЭ
Скачать материал
Скачать материал


- Сейчас обучается 46 человек из 28 регионов


- Сейчас обучается 104 человека из 46 регионов


- Сейчас обучается 97 человек из 42 регионов


Краткое описание документа:
В настоящее время важным фактором в обучении старшеклассников является подготовка их к ЕГЭ (ГИА). Моя методика подготовки основана на подаче базового и специфического теоретического материала и закреплении его на задачах в письменной и интерактивной форме, которая позволяет обеспечить прочное и осознанное усвоение знаний, умений и навыков, развитие способностей учащихся, приобщение их к творческой деятельности. Подача теории по физике должна даваться только учителем, который глубоко и качественно объяснит суть физических явлений, законов, понятий и т. д. Также необходимо показать учащимся алгоритмы решения основных тематических задач. А вот далее предоставляется свобода ученику в самостоятельной деятельности – повторении и воспроизведении теоретического материала, решении задач. Именно самостоятельная деятельность позволяет ученику раскрыться, лучше использовать свой творческий потенциал, научит применять теоретическую базу при решении различных задач.
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 153 784 материала в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Другие материалы
Презентация по физике -10 класс
- Учебник: «Физика. Базовый и углубленный уровни (в 2 частях) », Генденштейн Л.Э., Дик Ю.И.
- Тема: 1. Основные положения молекулярно-кинетической теории
- 19.12.2018
- 383
- 0



- 19.12.2018
- 3022
- 16
- 19.12.2018
- 2106
- 36

- 18.12.2018
- 475
- 1
Рейтинг:
2 из 5
- 18.12.2018
- 467
- 35

Вам будут интересны эти курсы:
-
Курс повышения квалификации «Информационные технологии в деятельности учителя физики»
-
Курс повышения квалификации «Правовое обеспечение деятельности коммерческой организации и индивидуальных предпринимателей»
-
Курс повышения квалификации «Основы управления проектами в условиях реализации ФГОС»
-
Курс повышения квалификации «Организация практики студентов в соответствии с требованиями ФГОС педагогических направлений подготовки»
-
Курс повышения квалификации «Организация практики студентов в соответствии с требованиями ФГОС юридических направлений подготовки»
-
Курс повышения квалификации «Применение MS Word, Excel в финансовых расчетах»
-
Курс профессиональной переподготовки «Организация менеджмента в туризме»
-
Курс повышения квалификации «ЕГЭ по физике: методика решения задач»
-
Курс профессиональной переподготовки «Управление сервисами информационных технологий»
-
Курс профессиональной переподготовки «Методика организации, руководства и координации музейной деятельности»
-
Курс профессиональной переподготовки «Осуществление и координация продаж»
-
Курс профессиональной переподготовки «Организация и управление процессом по предоставлению услуг по кредитному брокериджу»
-
Курс профессиональной переподготовки «Организация маркетинговой деятельности»
-
Настоящий материал опубликован пользователем Ишкина Надежда Анатольевна. Инфоурок является
информационным посредником и предоставляет пользователям возможность размещать на сайте
методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них
сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайтЕсли Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.Удалить материал
-
- На сайте: 4 года и 2 месяца
- Подписчики: 0
- Всего просмотров: 7889
-
Всего материалов:
6
Термодинамика. Работа в термодинамике, первый закон термодинамики, КПД тепловой машины
В. З. Шапиро
Девятое задание ЕГЭ по физике проверяет знания по разделам «Молекулярная физика» и «Термодинамика». Это задание базового уровня. В нём отсутствует возможность выбора ответа. Особое внимание надо уделить теме «Насыщенный пар. Относительная влажность воздуха». Качественное понимание всех происходящих процессов приведет к правильному решению задачи.
1. Относительная влажность воздуха в сосуде, закрытом поршнем, равна 40%. Во сколько раз необходимо уменьшить объём сосуда, чтобы водяной пар в нём стал насыщенным?
Ответ: в___________________________ раз(а).
Необходимая теория: Насыщенный пар
Относительная влажность равна 100% в случае, если водяной пар становится насыщенным. Увеличение влажности при постоянной температуре происходит из-за роста парциального давления водяного пара. Это давление растет с уменьшением объёма сосуда.
Относительная влажность равна 100% в случае, если водяной пар становится насыщенным. Увеличение влажности при постоянной температуре происходит из-за роста парциального давления водяного пара. Это давление растет с уменьшением объёма сосуда.
Отношение влажностей воздуха будет равно обратному отношению объемов сосуда.
Ответ: в 2,5 раза.
У идеального теплового двигателя Карно температура нагревателя 327°С, а температура холодильника 27°С. Определите КПД теплового двигателя.
Ответ: ___________________________ %.
Необходимая теория: Тепловые машины
Формула для расчета КПД идеальной машины имеет вид: подставим сюда данные из условия задачи, переведя температуру в градусы Кельвина.
Секрет решения: В формуле для расчета КПД идеальной тепловой машины необходимо переводить температуру в градусы Кельвина. Если в числителе разность температур по обеим шкалам одинаковая, то в знаменателе температура должна быть строго по абсолютной шкале.
3. На рисунке показан график изменения состояния постоянной массы одноатомного идеального газа. В этом процессе газ получил количество теплоты, равное 3 кДж. На сколько в результате этого увеличилась его внутренняя энергия?
Ответ: на ___________________________ кДж
Необходимая теория: Первый закон термодинамики
Для решения задачи необходимо применить первый закон термодинамики
Так как график проходит через начало координат, то он характеризует изохорный процесс (V = const). При этом процессе газ работу не совершает, работа внешних сил также равна нулю. Поэтому первый закон термодинамики принимает вид Так как газ получил 3 кДж теплоты, то оно полностью пошло на изменение его внутренней энергии.
Ответ: 3 кДж.
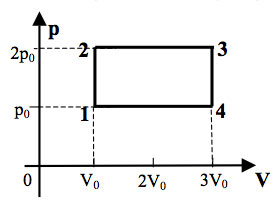
4. На pV-диаграмме (см. рисунок) показано, как изменялось давление газа при его переходе из состояния 1 в состояние 3. Каково отношение работ газа в процессах 1–2 и 2–3?
На pV-диаграмме работа, совершенная газом, численно равна площади под графиком. На участке 1-2 надо найти площадь прямоугольника, на участке 2-3 площадь трапеции.
Ответ: 0,5.
Понимание того, как термодинамические процессы изображаются на графиках, необходимо при решении задач, и особенно задач второй части. Любой график – это тот же самый текст, только имеющий другой вид (форму).
Благодарим за то, что пользуйтесь нашими материалами.
Информация на странице «Задание 9 ЕГЭ по физике» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать необходимые и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из данного раздела.
Публикация обновлена:
09.03.2023
Задачи из ДЕМОВАРИАНТОВ (с решениями)
1. Воздушный шар, оболочка
которого имеет массу М = 145 кг и объем V =
230 м3, наполняется горячим воздухом при нормальном
атмосферном давлении и температуре окружающего воздуха tо
= 0оС. Какую минимальную температуру t должен
иметь воздух внутри оболочки, чтобы шар начал подниматься? Оболочка
шара нерастяжима и имеет в нижней части небольшое отверстие.
Образец возможного решения
2. Воздушный
шар с газонепроницаемой оболочкой массой 400 кг заполнен гелием.
Он может удерживать в воздухе на высоте, где температура воздуха
17оС, а давление 105 Па, груз массой 225
кг. Какова масса гелия в оболочке шара? Считать, что оболочка
шара не оказывает сопротивления изменению объема шара.
Образец возможного решения
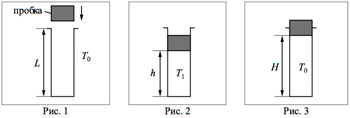
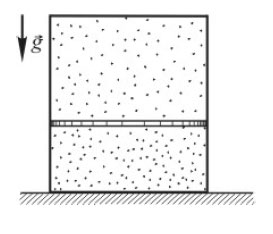
2*. В камере, заполненной азотом, при температуре T = 300 К находится открытый цилиндрический сосуд (см. рис. 1). Высота сосуда L = 50 см. Сосуд плотно закрывают цилиндрической пробкой и охлаждают до температуры T1. В результате расстояние от дна сосуда до низа пробки становится равным h = 40 см (см. рис. 2). Затем сосуд нагревают до первоначальной температуры T0. Расстояние от дна сосуда до низа пробки при этой температуре становится равным H = 46 см (см. рис. 3). Чему равна температура T1? Величину силы трения между пробкой и стенками сосуда считать одинаковой при движении пробки вниз и вверх. Массой пробки пренебречь. Давление азота в камере во время эксперимента поддерживается постоянным.
Образец возможного решения
3. В медный
стакан калориметра массой 200 г, содержащий 150 г воды, опустили
кусок льда, имевший температуру 0°С. Начальная температура калориметра
с водой 25°С. В момент времени, когда наступит тепловое равновесие,
температура воды и калориметра стала равной 5°С. Рассчитайте массу
льда. Удельная теплоемкость меди 390 Дж/кг•К, удельная теплоемкость
воды 4200 Дж/кг•К, удельная теплота плавления льда 3,35•105
Дж/кг. Потери тепла калориметром считать пренебрежимо малыми.
Образец возможного решения
4. Необходимо расплавить лёд массой 0,2 кг,
имеющий температуру 0оС. Выполнима ли эта задача,
если потребляемая мощность нагревательного элемента – 400 Вт,
тепловые потери составляют 30%, а время работы нагревателя не
должно превышать 5 минут?
Образец возможного решения
4*. Теплоизолированный горизонтальный сосуд разделён пористой перегородкой на две равные части. В начальный момент в левой части сосуда находится ν = 2 моль гелия, а в правой – такое же количество моль аргона. Атомы гелия могут проникать через перегородку, а для атомов аргона перегородка непроницаема. Температура гелия равна температуре аргона: Т = 300 К. Определите отношение внутренних энергий газов по разные стороны перегородки после установления термодинамического равновесия.
Образец возможного решения
4**. Теплоизолированный цилиндр разделён подвижным теплопроводным поршнем на две части. В одной части цилиндра находится гелий, а в другой – аргон. В начальный момент температура гелия равна 300 К, а аргона – 900 К; объёмы, занимаемые газами, одинаковы, а поршень находится в равновесии. Поршень медленно перемещается без трения. Теплоёмкость поршня и цилиндра пренебрежимо мала. Чему равно отношение внутренней энергии гелия после установления теплового равновесия к его энергии в начальный момент?
Образец возможного решения
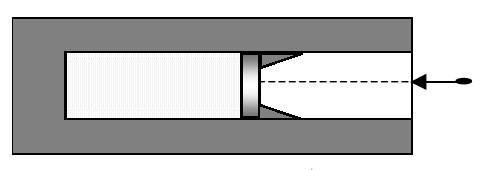
5. В вакууме
закреплен горизонтальный цилиндр с поршнем. В цилиндре находится
0,1 моль гелия. Поршень удерживается упорами и может скользить
влево вдоль стенок цилиндра без трения. В поршень попадает пуля
массой 10 г, летящая горизонтально со скоростью 400 м/с, и застревает
в нем. Температура гелия в момент остановки поршня в крайнем левом
положении возрастает на 64 К. Какова масса поршня? Считать, что
за время движения поршня газ не успевает обменяться теплом с поршнем
и цилиндром.
Образец возможного решения
6. В горизонтальном цилиндрическом сосуде,
закрытом поршнем, находится одноатомный идеальный газ. Первоначальное
давление газа p1 = 4•105
Па. Расстояние от дна сосуда до поршня равно L. Площадь
поперечного сечения поршня S = 25 см2. В
результате медленного нагревания газ получил количество теплоты
Q = 1,65 кДж, а поршень сдвинулся на расстояние x
= 10 см. При движении поршня на него со стороны стенок сосуда
действует сила трения величиной Fтр = 3•103
Н. Найдите L. Считать, что сосуд находится в вакууме.
Образец возможного решения
7. На pT-диаграмме показан
цикл тепловой машины, у которой рабочим телом является идеальный
газ (см. рисунок). На каком из участков цикла 1 – 2, 2 – 3, 3
– 4, 4 – 1 работа газа наибольшая по модулю?
Образец возможного решения
8. 10 моль одноатомного идеального
газа сначала охладили, уменьшив давление в 3 раза, а затем нагрели
до первоначальной температуры 300 К (см. рисунок). Какое количество
теплоты получил газ на участке 2 — 3?
Образец возможного решения
9. 10 моль идеального одноатомного газа охладили,
уменьшив давление в 3 раза. Затем газ нагрели до первоначальной
температуры 300 К (см. рисунок). Какое количество теплоты сообщено
газу на участке 2 — 3?
Образец возможного решения
10. 1 моль идеального одноатомного газа сначала
охладили, а затем нагрели до первоначальной температуры 300
К, увеличив объем газа в 3 раза (см. рисунок). Какое количество
теплоты отдал газ на участке 1 — 2?
Образец возможного решения
10*. Над одноатомным идеальным газом проводится циклический процесс, показанный на рисунке. На участке 1–2 газ совершает работу А12 = 1000 Дж. На адиабате 3–1 внешние силы сжимают газ, совершая работу |A31| = 370 Дж. Количество вещества газа в ходе процесса не меняется. Найдите количество теплоты |Qхол|, отданное газом за цикл холодильнику.
Образец возможного решения
11. Рассчитайте КПД тепловой
машины, использующей в качестве рабочего тела одноатомный идеальный
газ и работающей по циклу, изображенному на рисунке.
Образец возможного решения
Избранные задачи прошлых лет (с ответами)
12. Вертикально расположенный
замкнутый цилиндрический сосуд высотой 50 см разделен подвижным
поршнем весом 110 Н на две части, в каждой из которых содержится
одинаковое количество идеального газа при температуре 361 К. Сколько
молей газа находится в каждой части цилиндра, если поршень находится
на высоте 20 см от дна сосуда? Толщиной поршня пренебречь.
13. В калориметре
находился лед при температуре t1 = — 5 °С.
Какой была масса m1 льда, если после добавления
в калориметр m2 = 4 кг воды, имеющей температуру
t2 = 20 °С, и установления теплового равновесия
температура содержимого калориметра оказалась равной t
= 0 °С, причем в калориметре была только вода?
14. Теплоизолированный
цилиндр разделен подвижным теплопроводным поршнем на две части.
В одной части цилиндра находится гелий, а в другой — аргон. В
начальный момент температура гелия равна 300 К, а аргона — 900
К. При этом объемы, занимаемые газами одинаковы. Какую температуру
будут иметь газы в цилиндре после установления теплового равновесия,
если поршень перемещается без трения? Теплоемкостью сосуда и поршня
пренебречь.
15. Теплоизолированный
сосуд объемом V = 2 м3 разделен теплопроводящей
перегородкой на две части одинакового объема. В одной части находится
m = 1 кг гелия, а в другой части m = 1 кг аргона.
Средняя квадратичная скорость атомов аргона равна средней квадратичной
скорости атомов гелия и составляет υ = 500 м/с. Рассчитайте
парциальное давление гелия после удаления перегородки.
16. Теплоизолированный
сосуд объемом V = 2 м3 разделен пористой перегородкой
на две равные части. В начальный момент в одной части сосуда находится
νHe = 2 моль гелия, а в другой – νAr
= 1 моль аргона. Температура гелия ТHe = 300
К, а температура аргона ТAr = 600 К. Атомы
гелия могут свободно проникать через поры в перегородке, а атомы
аргона – нет. Определите температуру гелия после установления
теплового равновесия в системе.
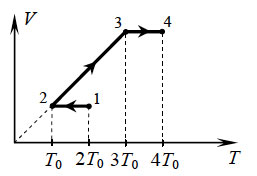
17. С одним молем идеального
одноатомного газа совершают процесс 1-2-3-4, показанный на рисунке
в координатах V-Т. Во сколько раз количество теплоты,
полученное газом в процессе 1-2-3-4 больше работы газа в этом
процессе?
18. Один моль одноатомного
идеального газа совершает процесс 1-2-3 (см. рисунок). На участке
2 — 3 к газу подводят 3 кДж теплоты. Т0 =
100 К. Найдите отношение работы, совершаемой газом в ходе всего
процесса А123, к соответствующему полному
количеству подведенной к нему теплоты Q123.
19. Один моль идеального
одноатомного газа сначала изотермически сжали (Т1
= 300 К). Затем газ изохорно охладили, понизив давление в 3 раза
(см. рисунок). Какое количество теплоты отдал газ на участке 2
— 3?
20. Идеальный одноатомный
газ расширяется сначала адиабатно, а затем изобарно. Конечная
температура газа равна начальной (см. рисунок). За весь процесс
1-2-3 газом совершается работа, равная 5 кДж. Какую работу совершает
газ при адиабатном расширении?
21. На рисунке в координатах
p,T показан цикл тепловой машины, у которой
рабочим телом является идеальный газ. На каком участке цикла работа
газа наименьшая по модулю?
22. Один моль одноатомного
идеального газа совершает цикл, изображенный на pV-диаграмме
(см. рисунок). Участок 1 – 2 –– изотерма, 2 – 3 –– изобара, 3
– 1 –– адиабата. Работа, совершаемая газом за цикл, равна А.
Разность температур в состояниях 1 и 3 составляет ΔТ.
Какую работу совершает газ при изотермическом процессе?
23. Газообразный гелий находится
в цилиндре под подвижным поршнем. Газ сжимают в адиабатическом
процессе, переводя его из состояния 1 в состояние 2 (см. рис.).
Над газом совершается при этом работа сжатия А12
(А12> 0). Затем газ расширяется в изотермическом
процессе 2-3, и, наконец, из состояния 3 газ переводят в состояние
1 в процессе, когда его давление Р прямо пропорционально
объему V. Найти работу А23, которую
совершил газ в процессе изотермического расширения, если во всем
замкнутом цикле 1-2-3-1 он совершил работу А.
24. Температура
гелия увеличилась в k = 3 раза в процессе P2V
= const (Р — давление, V — объем газа), а его
внутренняя энергия изменилась на 100 Дж. Найти: 1) начальный объем
V1 газа; 2) начальное давление P1
газа. Максимальный объем, который занимал газ в процессе нагрева,
равнялся Vmax = 3 л.
25. Одноатомный идеальный
газ неизменной массы совершает циклический процесс, показанный
на рисунке. За цикл от нагревателя газ получает количество теплоты
QH = 8 кДж. Чему равна работа газа за цикл?
прошлых лет
Работа в термодинамике
В термодинамике, в отличие от механики, рассматривается не движение тела как целого, а лишь относительное изменение частей термодинамической системы, в результате которого меняется ее объем.
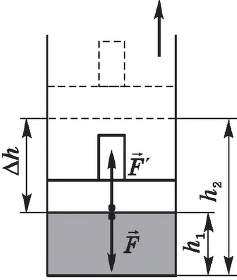
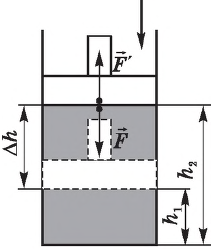
Рассмотрим работу газа при изобарическом расширении.
Вычислим работу, совершаемую газом при его действии на поршень с силой ${F’}↖{→}$, равной по величине и противоположной по направлению силе ${F’}↖{→}$, действующей на газ со стороны поршня: ${F’}↖{→}=-{F’}↖{→}$ (согласно третьему закону Ньютона), $F’=pS$, где $p$ — давление газа, а $S$ — площадь поверхности поршня. Если перемещение поршня $∆h$ в результате расширения мало, то давление газа можно считать постоянным и работа газа равна:
$A’=F’∆h=pS∆h=p∆V$
Если газ расширяется, он совершает положительную работу, та к как перемещение поршня совпадает по направлению с силой ${F’}↖{→}$. Если газ сжимается, то работа газа отрицательна, поскольку перемещение поршня противоположно силе ${F’}↖{→}$. В формуле $A’=F’∆h=pS∆h=p∆V$ появится знак «минус»: $∆V < 0$, поскольку $∆h < 0$.
Работа внешних сил $А$, наоборот, положительна при сжатии газа и отрицательна при расширении:
$A=-A’=-p∆V$
Совершая над газом положительную работу, внешние тела передают ему часть своей энергии. При расширении газа внешние тела отбирают у газа часть его энергии — работа внешних сил отрицательна.
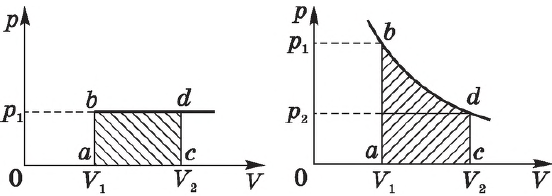
На графике зависимости давления от объема $р(V)$ работа определяется как площадь, ограниченная кривой $р(V)$, осью $V$ и отрезками $ab$ и $cd$, равными давлениям $р_1$ в начальном ($V_1$) и $р_2$ в конечном ($V_2$) состояниях, как для изобарного, так и для изотермического процессов.
Первый закон термодинамики
Первое начало (первый закон) термодинамики — это закон сохранения и превращения энергии для термодинамической системы.
Согласно первому началу термодинамики, работа может совершаться только за счет теплоты или какой-либо другой формы энергии. Следовательно, работу и количество теплоты измеряют в одних единицах — джоулях (как и энергию).
Первое начало термодинамики было сформулировано немецким ученым Ю. Л. Майером в 1842 г. и подтверждено экспериментально английским ученым Дж. Джоулем в 1843 г.
Первый закон термодинамики формулируется так:
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
$∆U=A+Q$
где $∆U$ — изменение внутренней энергии, $А$ — работа внешних сил, $Q$ — количество теплоты, переданной системе.
Из $∆U=A+Q$ следует закон сохранения внутренней энергии. Если систему изолировать от внешних воздействий, $A=0$ и $Q=0$,а следовательно, $∆U=0$.
При любых процессах, происходящих в изолированной системе, ее внутренняя энергия остается постоянной.
Если работу совершает система, а не внешние силы, то уравнение ($∆U=A+Q$) записывается в виде:
$Q=∆U+A’$
где $А’$ — работа, совершаемая системой ($А’=-А$).
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Первое начало термодинамики может быть сформулировано как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника, т. е. только за счет внутренней энергии.
Действительно, если к телу не поступает теплота ($Q=0$), то работа $А’$, согласно уравнению $Q=∆U+A’$, совершается только за счет убыли внутренней энергии $A’=-∆U$. После того, как запас энергии окажется исчерпанным, двигатель перестает работать.
Следует помнить, что как работа, так и количество теплоты являются характеристиками процесса изменения внутренней энергии, поэтому нельзя говорить, что в системе содержится определенное количество теплоты или работы. Система в любом состоянии обладает лишь определенной внутренней энергией.
Применение первого закона термодинамики к различным процессам
Рассмотрим применение первого закона термодинамики к различным термодинамическим процессам.
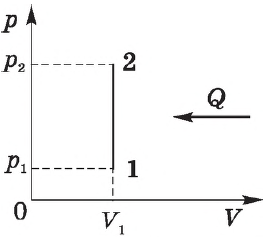
Изохорный процесс. Зависимость $р(Т)$ на термодинамической диаграмме изображается изохорой.
Изохорный (изохорический) процесс — термодинмический процесс, происходящий в системе при постоянном объеме.
Изохорный процесс можно осуществить в газах и жидкостях, заключенных в сосуд с постоянным объемом.
При изохорном процессе объем газа не меняется ($∆V=0$), и, согласно первому началу термодинамики $Q=∆U+A’$,
$∆U=Q$
т. е. изменение внутренней энергии равно количеству переданного тепла, т. к. работа ($A=p∆V=0$) газом не совершается.
Если газ нагревается, то $Q > 0$ и $∆U > 0$, его внутренняя энергия увеличивается. При охлаждении газа $Q < 0$ и $∆U < 0$, внутренняя энергия уменьшается.
Изотермический процесс графически изображается изотермой.
Изотермический процесс — это термодинамический процесс, происходящий в системе при постоянной температуре.
Поскольку при изотермическом процессе внутренняя энергия газа не меняется ($T=const$), то все переданное газу количество теплоты идет на совершение работы:
$Q=A’$
При получении газом теплоты ($Q > 0$) он совершает положительную работу ($А’ > 0$). Если газ отдает тепло окружающей среде, $Q < 0$ и $А’ < 0$. В этом случае над газом совершается работа внешними силами. Для внешних сил работа положительна. Геометрически работа при изотермическом процессе определяется площадью под кривой $р(V)$.
Изобарный процесс на термодинамической диаграмме изображается изобарой.
Изобарный (изобарический) процесс — термодинамический процесс, происходящий в системе с постоянным давлением $p$.
Примером изобарного процесса является расширение газа в цилиндре со свободно ходящим нагруженным поршнем.
При изобарном процессе согласно формуле $Q=∆U+A’$ передаваемое газу количество теплоты идет на изменение его внутренней энергии $∆U$ и на совершение им работы $A’$ при постоянном давлении:
$Q=∆U+A’$
Работа идеального газа определяется по графику зависимости $p(V)$ для изобарного процесса ($A’=p∆V$).
Для идеального газа при изобарном процессе объем пропорционален температуре, в реальных газах часть теплоты расходуется на изменение средней энергии взаимодействия частиц.
Адиабатический процесс
Адиабатический процесс (адиабатный процесс) — это термодинамический процесс, происходящий в системе без теплообмена с окружающей средой ($Q=0$).
Адиабатическая изоляция системы приближенно достигается в сосудах Дьюара, в так называемых адиабатных оболочках. На адиабатически изолированную систему не оказывает влияния изменение температуры окружающих тел. Ее внутренняя энергия и может меняться только за счет работы, совершаемой внешними телами над системой, или самой системой.
Согласно первому началу термодинамики ($∆U=A+Q$), в адиабатной системе
$∆U=A$
где $А$ — работа внешних сил.
При адиабатном расширении газа $А < 0$.
Следовательно,
$∆U={i}/{2}·{m}/{M}R∆T < 0,$
что означает уменьшение температуры при адиабатном расширении. Оно приводит к тому, что давление газа уменьшается более резко, чем при изотермическом процессе.
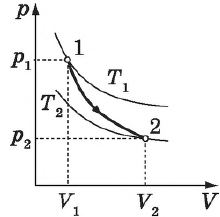
На рисунке адиабата $1—2$, проходящая между двумя изотермами, наглядно иллюстрирует сказанное. Площадь под адиабатой численно равна работе, совершаемой газом при его адиабатическом расширении от объема $V_1$ до $V_2$.
Адиабатное сжатие приводит к повышению температуры газа, т. к. в результате упругих соударений молекул газа с поршнем их средняя кинетическая энергия возрастает, в отличие от расширения, когда она уменьшается (в первом случае скорости молекул газа увеличиваются, во втором — уменьшаются).
Резкое нагревание воздуха при адиабатическом сжатии используется в двигателях Дизеля.
Принцип действия тепловых двигателей
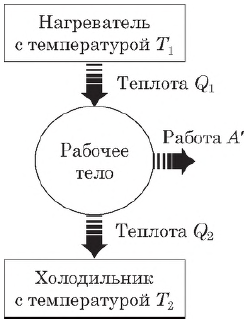
Тепловой двигатель — это устройство, преобразующее внутреннюю энергию топлива в механическую энергию.
Согласно второму началу термодинамики, тепловой двигатель может непрерывно совершать периодически повторяющуюся механическую работу за счет охлаждения окружающих тел, если он не только получает теплоту от более горячего тела (нагревателя), но при этом отдает теплоту менее нагретому телу (холодильнику). Следовательно, на совершение работы идет не все количество теплоты, полученное от нагревателя, а только часть ее.
Таким образом, основными элементами любого теплового двигателя являются:
- рабочее тело (газ или пар), совершающее работу;
- нагреватель, сообщающий энергию рабочему телу;
- холодильник, поглощающий часть энергии от рабочего тела.
Коэффициент полезного действия теплового двигателя
Согласно закону сохранения энергии, работа, совершаемая двигателем, равна:
$A’=|Q_1|-|Q_2|$
где $Q_1$ — количество теплоты, полученное от нагревателя, $Q_2$ — количество теплоты, отданное холодильнику.
Коэффициентом полезного действия (КПД) теплового двигателя называется отношение работы $А’$, совершаемой двигателем, к количеству теплоты, полученному от нагревателя:
$η={A’}/{|Q_1|}={|Q_1|-|Q_2|}/{|Q_1|}=1-{|Q_2|}/{|Q_1|}$
Так как у всех двигателей некоторое количество теплоты передается холодильнику, то $η < 1$.
КПД теплового двигателя пропорционален разности температур нагревателя и холодильника. При $T_1 — T_2=0$ двигатель не может работать.
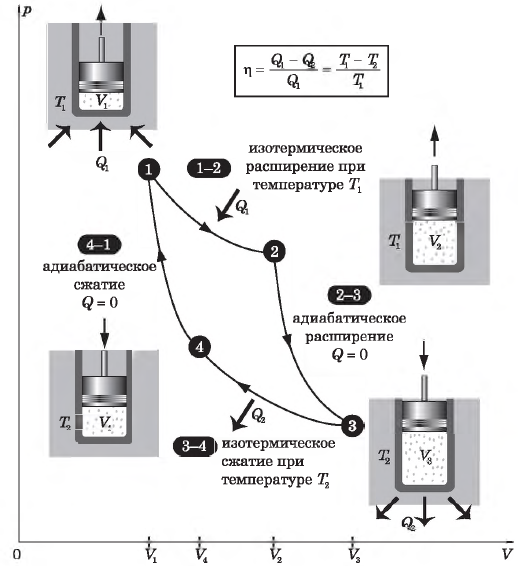
Цикл Карно
Цикл Карно — это круговой обратимый процесс, состоящий из двух изотермических и двух адиабатических процессов.
Впервые этот процесс был рассмотрен французским инженером и ученым Н. Л. С. Карно в 1824 г. в книге «Размышления о движущей силе огня и о машинах, способных развивать эту силу».
Целью исследований Карно было выяснение причин несовершенства тепловых машин того времени (они имели КПД $< 5%$)и поиски путей их усовершенствования.
Выбор двух изотермических и двух адиабатических процессов был обусловлен тем, что работа газа при изотермическом расширении совершается за счет внутренней энергии нагревателя, а при адиабатном процессе — за счет внутренней энергии расширяющегося газа. В этом цикле исключен контакт тел с разной температурой, следовательно, исключена теплопередача без совершения работы.
Цикл Карно — самый эффективный из всех возможных. Его КПД максимален.
На рисунке изображены термодинамические процессы цикла. В процессе изотермического расширения ($1-2$) при температуре $Т_1$ работа совершается за счет изменения внутренней энергии нагревателя, т. е. за счет подведения к газу количества теплоты $Q_1$:
$A_{12}=Q_1.$ Охлаждение газа перед сжатием ($3-4$) происходит при адиабатном расширении ($2-3$). Изменение внутренней энергии $∆U_{23}$ при адиабатном процессе ($Q=0$) полностью преобразуется в механическую работу:
$A_{23}=-∆U_{23}$
Температура газа в результате адиабатического расширения ($2-3$) понижается до температуры холодильника $Т_2 < Т_1$. В процессе ($3-4$) газ изотермически сжимается, передавая холодильнику количество теплоты $Q_2$:
$A_{34}=Q_2,$
Цикл завершается процессом адиабатического сжатия ($4—1$), при котором газ нагревается до температуры $Т_1$.
Максимальное значение КПД тепловых двигателей, работающих на идеальном газе, по циклу Карно:
$η={T_1-T_2}/{T_1}=1-{T_2}/{T_1}$
Суть формулы $η={T_1-T_2}/{T_1}=1-{T_2}/{T_1}$ выражена в доказанной С. Карно теореме о том, что КПД любого теплового двигателя не может превышать КПД цикла Карно, осуществляемого при той же температуре нагревателя и холодильника.