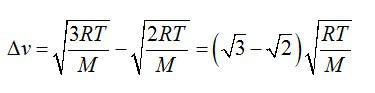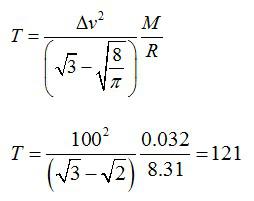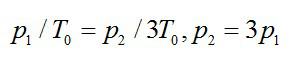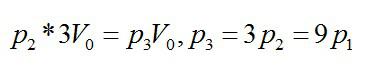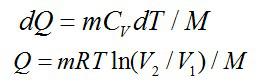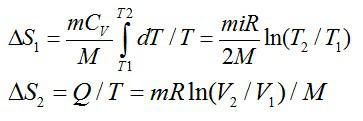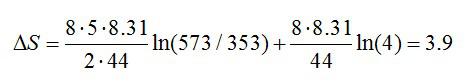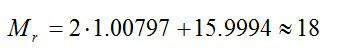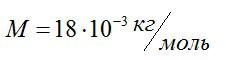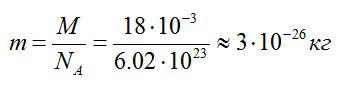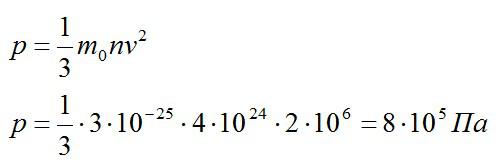Пройти тестирование по этим заданиям
Вернуться к каталогу заданий
Версия для печати и копирования в MS Word
1
Задания Д5 B8 № 826
Одним из подтверждений положения молекулярно-кинетической теории строения вещества о том, что частицы вещества хаотично движутся, может служить:
A. Возможность испарения жидкости при любой температуре.
Б. Зависимость давления столба жидкости от глубины.
B. Выталкивание из жидкости погруженных в нее тел.
Какие из утверждений правильны?
1) только А
2) только Б
3) только А и Б
4) только Б и В
2
Задания Д5 B8 № 3206
Чем можно объяснить, что через некоторое время после открытия в комнате флакона с духами их запах ощущается по всему помещению?
1) Диффузией газов
2) Теплопроводностью стенок флакона
3) Духи могут действовать на рецепторы носа на расстоянии
4) Духи в открытом флаконе испускают излучение, улавливаемое рецепторами носа
3
Задания Д5 B8 № 3216
Идеальный газ, находящийся в закрытом сосуде, оказывает давление на его стенки. Это объясняется тем что
1) молекулы прилипают к стенкам сосуда
2) идеальный газ имеет большую плотность
3) молекулы газа передают стенкам энергию
4) молекулы газа передают стенкам импульс
4
Задания Д5 B8 № 3288
При понижении температуры газа в запаянном сосуде давление газа уменьшается. Это уменьшение давления объясняется тем, что
1) уменьшается объём сосуда за счет остывания его стенок
2) уменьшается энергия теплового движения молекул газа
3) уменьшаются размеры молекул газа при его охлаждении
4) уменьшается энергия взаимодействия молекул газа друг с другом
5
Задания Д5 B8 № 3300
Отвечая на вопрос учителя, Сережа, используя положения МКТ, указал следующие характеристики теплового движения молекул вещества:
A) в веществе каждая молекула движется с присущей ей скоростью, которая не меняется с течением времени;
Б) не бывает резкого изменения по модулю или направлению скорости какой-либо молекулы вещества;
B) среднее число молекул, у которых значение модуля скорости больше 300 м/с, но меньше 350 м/с, не меняется с течением времени;
Г) среднее значение модуля скоростей всех молекул вещества не меняется с течением времени.
Какие из этих признаков Сережа указал правильно (считая, что температура вещества постоянна)?
1) А и Б
2) В и Г
3) А и В
4) Б и Г
Пройти тестирование по этим заданиям
Задачи по молекулярной физике с решениями
Элементы молекулярной физики. Основное уравнение молекулярно-кинетической теории (МКТ)
4.1.1 В баллоне находится 20 моль газа. Сколько молекул газа находится
4.1.2 Определить массу молекулы кислорода
4.1.3 Сколько молекул содержится в 5 кг кислорода?
4.1.4 При температуре 320 К средняя квадратичная скорость молекулы кислорода 500 м/с
4.1.5 Определить давление водорода, если средняя квадратичная скорость его молекул
4.1.6 Какова средняя кинетическая энергия поступательного движения молекул газа
4.1.7 Определить давление, при котором 1 м3 газа, имеющий температуру 60 C, содержит
4.1.8 Сколько молекул содержится в 1 л воды?
4.1.9 Какое значение температуры по шкале Кельвина соответствует температуре 100 C?
4.1.10 Какой объем при нормальных условиях занимают 5 г углекислого газа?
4.1.11 Чему равна температура газа, если при концентрации 2,65×10^25 м^(-3) он создает
4.1.12 Определить число молекул, содержащихся в 1 г воды
4.1.13 Определить количество вещества, содержащегося в медной отливке массой 96 кг
4.1.14 В комнате размером 4x5x2,7 м^3 испарился кристаллик йода массой 20 мг. Сколько
4.1.15 В лабораторных условиях создан высокий вакуум, то есть очень малое давление
4.1.16 Определить молярную массу газа, если его плотность при нормальных условиях
4.1.17 Найти число молекул в 2 кг углекислого газа
4.1.18 Во сколько раз масса молекулы углекислого газа CO2 больше массы молекулы аммиака NH3
4.1.19 За 20 суток из стакана полностью испарилась 0,2 кг воды. Сколько в среднем молекул
4.1.20 Считая, что диаметр молекул водорода составляет около 0,23 нм, подсчитать, какой длины
4.1.21 В сосуде находится газ под давлением 150 кПа при температуре 23 C. Найти
4.1.22 Определить среднюю квадратичную скорость молекул водорода
4.1.23 Под каким давлением находится кислород в баллоне, если при температуре 27 C
4.1.24 При какой температуре средняя квадратичная скорость молекул кислорода
4.1.25 Какова плотность сжатого воздуха при 0 C в камере шины автомобиля “Волга”? Давление
4.1.26 Определить среднюю квадратичную скорость молекул азота при температуре
4.1.27 Определить плотность воздуха при нормальных условиях. Молярную массу принять
4.1.28 Каково давление азота, если его плотность равна 1,35 кг/м^3, а средняя квадратичная
4.1.29 Сколько молекул кислорода находится в сосуде объемом 1 л, если температура
4.1.30 Определить плотность воздуха при 27 C и давлении 0,1 МПа
4.1.31 Какое давление на стенки сосуда производят молекулы газа, если масса газа 3 г, объем
4.1.32 Какое давление производит углекислый газ при температуре 330 К, если его плотность
4.1.33 Вычислить среднюю квадратичную скорость молекул углекислого газа
4.1.34 Определить среднеквадратичную скорость молекул газа при давлении 100 кПа и плотности
4.1.35 В баллоне емкостью 40 л находится 10 кг кислорода под давлением 20 МПа. Найти
4.1.36 Энергия поступательного движения, которой обладают все молекулы газа, находящегося
4.1.37 Найти концентрацию молекул газа, у которого средняя квадратичная скорость молекул
4.1.38 В первом сосуде находится азот, во втором – водород. Чему равно отношение давления
4.1.39 В сосуде вместимостью 2 м3 находится 2,4 кг газа. Под каким давлением находится газ
4.1.40 Плотность газа в баллоне электрической лампы 0,9 кг/м3, давление при горении 110 кПа
4.1.41 При какой температуре находится одноатомный газ, если средняя кинетическая энергия
4.1.42 Под каким давлением находится кислород в баллоне, если при температуре 27 C
4.1.43 Найдите отношение средних скоростей молекул O2 и H2 при одинаковой температуре
4.1.44 Найти среднюю квадратичную скорость молекул газа, имеющего плотность 1,8 кг/м3
4.1.45 В баллоне находится кислород при давлении 4 МПа и температуре 42 C. Определить
4.1.46 В баллоне объемом 0,01 м3 находится газ, кинетическая энергия поступательного движения
4.1.47 Во сколько раз плотность метана (CH4) отличается от плотности кислорода (O2)
4.1.48 Определить давление азота в ампуле, если при 0 C в ней концентрация молекул
4.1.49 Во сколько раз средняя квадратичная скорость молекул воздуха при температуре 303 К
4.1.50 При некоторой температуре средняя скорость молекул азота равна 600 м/с. Какова
4.1.51 До какой температуры при нормальном атмосферном давлении надо нагреть кислород
4.1.52 Во сколько раз плотность воздуха зимой при температуре минус 23 C больше плотности
4.1.53 Во сколько раз изменится средняя квадратичная скорость теплового движения молекул
4.1.54 Во сколько раз изменится средняя квадратичная скорость молекул идеального газа
4.1.55 Гелий находится при температуре 580 К. При какой температуре должен находиться
4.1.56 Во сколько раз изменится плотность молекул газа, если при увеличении температуры
4.1.57 Каким давлением нужно сжать воздух, чтобы при температуре 100 C его плотность стала
4.1.58 Среднеквадратичная скорость молекул газа равна 500 м/с. Какой объем займет газ массой
4.1.59 Оценить минимальное расстояние между центрами соседних атомов железа, считая его
4.1.60 Какое время понадобится для того, чтобы на поверхность стекла нанести слой серебра
4.1.61 Концентрация молекул кислорода (M=32 г/моль) в сосуде вместимостью 5 л равна
4.1.62 Если m0 – масса одной молекулы газа, N – общее число молекул газа, а NА – число Авогадро
4.1.63 Если m – масса газа, M – молярная масса газа, а NА – число Авогадро, то по какой формуле
4.1.64 Какое количество вещества содержится в алюминиевой ложке массы 27 г? Относительная
4.1.65 Чему равно среднее расстояние между молекулами насыщенного водяного пара при
4.1.66 Молекула двухатомного газа содержит 16 протонов и 16 нейтронов. Чем равна плотность
4.1.67 В сосуде вместимостью 4 м3 находится 4,8 кг идеального газа. Средняя квадратичная
4.1.68 В сосуде под давлением 10^5 Па плотность идеального газа составляет 1,2 кг/м3. Чему
4.1.69 Если температура идеального газа уменьшится в 4 раза, то во сколько раз изменится
4.1.70 По какой формуле можно рассчитать давление газа через его температуру T
4.1.71 Если M – молярная масса, m0 – масса молекулы, а v^2 – средний квадрат скорости молекул
4.1.72 В 1 см3 объема при давлении 20 кПа находятся 5×10^19 атомов гелия (молярная масса гелия
4.1.73 Если температура идеального газа возрастает в 2 раза, то как изменяется среднеквадратичная
4.1.74 Каким выражением определяется суммарная кинетическая энергия поступательного
4.1.75 В 1 дм3 объема при давлении 10^5 Па находятся 3×10^21 молекул кислорода (молярная
Уравнение Клапейрона-Менделеева
4.2.1 Какой объем занимает 1 кг кислорода при 0 C и давлении 800 кПа?
4.2.2 Найти массу углекислого газа в баллоне вместимостью 40 л при температуре 288 К и
4.2.3 В баллоне емкостью 25,6 л находится 1,04 кг азота при давлении 3,55 МПа. Определите
4.2.4 Баллон содержит 28 кг кислорода при давлении 770 кПа. Какова масса гелия, занимающего
4.2.5 В изотермическом процессе объем газа уменьшился вдвое. Во сколько раз
4.2.6 Некоторая масса газа при давлении 126 кПа и температуре 295 К занимает объем 500 л
4.2.7 Сколько молекул хлора содержится при нормальных условиях в колбе емкостью 0,5 л?
4.2.8 До какой температуры нужно нагреть запаянный шар, содержащий 9 г воды, чтобы шар
4.2.9 Сколько молекул воздуха содержится в комнате объемом 60 м3 при нормальных
4.2.10 Сколько весит воздух, занимающий объем 150 л при температуре 15 C и давлении
4.2.11 В баллоне емкостью 4 л создано давление 0,1 мкПа. Сколько молекул газа содержится
4.2.12 Баллон емкостью 40 л содержит 2,6 кг кислорода. При какой температуре возникает
4.2.13 Найти концентрацию молекул газа, если в баллоне емкостью 4 л создано давление
4.2.14 Сколько молекул ртути содержится в 1 м3 воздуха в помещении, зараженном ртутью
4.2.15 В баллоне емкостью 40 л содержится 1,98 кг углекислого газа при 0 С. При повышении
4.2.16 Баллон содержит 50 л кислорода, температура 27 C, давление 2 МПа. Найти массу
4.2.17 Сколько молекул газа заключено в объеме 0,5 м3, если он при температуре 300 К
4.2.18 В баллоне для сжиженных газов находится 4,2 кг метана (CH4) при давлении 1 МПа
4.2.19 В 1 м3 газа при давлении 120 кПа содержится 2×10^25 молекул, средняя квадратичная
4.2.20 Найти массу водорода, находящегося в баллоне объемом 20 л под давлением 830 кПа
4.2.21 Газ массой 16 г при давлении 1 МПа и температуре 112 C занимает объем 1600 см3
4.2.22 Найти число молекул воздуха в комнате, имеющей объем 8x5x4 м3, при температуре 10 C
4.2.23 Вычислить молярную массу бутана, 2 л которого при температуре 15 C и давлении 87 кПа
4.2.24 Какая часть газа осталась в баллоне, давление в котором было 12,2 МПа, а температура
4.2.25 Идеальный газ при давлении 1,33 кПа и температуре 15 C занимает объем 2 л. Каким
4.2.26 Из баллона емкостью 5 л из-за неисправности вентиля произошла утечка газа, в результате
4.2.27 Газ, объем которого 0,8 м3 при температуре 300 К производит давление 280 кПа. На сколько
4.2.28 В баллоне объемом 200 л при температуре 20 C и давлении 10 МПа находится кислород
4.2.29 Некоторый газ массой 7 г, находящийся в баллоне при температуре 27 C, создает давление
4.2.30 Сколько молекул воздуха выходит из комнаты объемом 80 м3 при повышении температуры
4.2.31 В цилиндре дизеля воздух сжимается от 80 до 3000 кПа, а объем уменьшается от 7,5 до 0,5 л
4.2.32 В открытом сосуде газ нагрели так, что его температура увеличилась в 3 раза. Сколько
4.2.33 Температура воздуха в комнате была 10 C. После того как печь протопили, температура
4.2.34 Газ массой 1,2 г занимает объем 400 см3 при температуре 280 К. После нагревания газа
4.2.35 Из баллона со сжатым водородом объемом 0,01 м3 вытекает газ, при температуре 280 К
4.2.36 Откачанная лампа накаливания объемом 10 см3 имеет трещину, в которую проникает
4.2.37 Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%
4.2.38 При температуре 727 C газ занимает объем 8 л и производит давление 200 кПа на стенки
4.2.39 Воздух в открытом сосуде нагревают от 10 до 600 C и затем, герметически закрыв сосуд
4.2.40 До какой температуры нагрели колбу, содержащую воздух, если давление воздуха в ней
4.2.41 Баллон, содержащий 1 кг азота, при испытании взорвался при температуре 630 К. Какое
4.2.42 При какой температуре давление 240 л водорода равно 126,6 кПа, если при нормальных
4.2.43 В баллоне находилось 5 кг газа при давлении 1 МПа. Какое количество газа взяли из баллона
4.2.44 Во сколько раз изменится объем кислорода массой 0,32 кг, если его давление увеличится
4.2.45 Баллон содержит газ при температуре 7 C и давлении 91,2 МПа. Каким будет давление
4.2.46 В баллоне находится газ при температуре 15 C. Во сколько раз изменится его давление
4.2.47 Сколько электронов заключается в 1 л кислорода при давлении 1 МПа и температуре
4.2.48 Плотность пара некоторого соединения углерода с водородом равна 3 г/л при 43 C
4.2.49 В комнате объемом в 30 м3 температура с 15 C поднялась до 25 C. На сколько при этом
4.2.50 Баллон содержит сжатый газ при 27 C и давлении 3 МПа. Каково будет давление, если
4.2.51 На сколько уменьшится масса воздуха в открытом сосуде, если его нагреть от 0 до 100 C?
4.2.52 Баллон содержит сжатый газ при 27 C и давлении 2000 кПа. Каково будет давление, если
4.2.53 Перед проведением газосварочных работ манометр баллона с кислородом показывал
4.2.54 Газ при давлении 126,6 кПа и температуре 300 К занимает объем 0,6 м3. Найти объем
4.2.55 Газ при давлении 0,2 МПа и температуре 15 C имеет объем 5 л. Чему равен объем
4.2.56 Сосуд вместимостью 0,6 м3, содержащий гелий массой 2 кг, разорвался при температуре
4.2.57 В сосуде объемом 10 литров находится 2 г водорода при температуре 2000 К. Определить
4.2.58 Какова минимальная разница в массе воздуха зимой и летом при нормальном атмосферном
4.2.59 Воздух в сосуде объемом 5 л находится при температуре 27 C под давлением 2 МПа
4.2.60 Некоторая масса водорода находится при температуре 200 К и давлении 0,4 кПа. Газ
4.2.61 Перед проведением газосварочных работ манометр баллона с кислородом показывал
4.2.62 В сосуде находится 1 литр воды при температуре 27 C. Чему стало бы равным давление
4.2.63 В двух сосудах находится одинаковое количество одного и того же газа. В первом сосуде
4.2.64 Резиновая камера содержит воздух при температуре 27 C и нормальном атмосферном
4.2.65 В баллоне объемом 10 л находится кислород, масса которого 12,8 г. Давление в баллоне
4.2.66 Баллон содержит 0,3 кг гелия. Абсолютная температура в баллоне уменьшилась на 10%
4.2.67 В откачанной ампуле объемом 3 см3 содержится радий массой 5 г в течение одного года
4.2.68 Два сосуда, содержащих одинаковую массу одного и того же газа, соединены трубкой
4.2.69 Сколько молей газа следует добавить к одному молю данного газа, чтобы его давление
4.2.70 В открытом цилиндре находится 90 г газа. Температуру газа увеличили от 300 до 450 К
4.2.71 Из баллона объемом 200 дм3, содержащего гелий при давлении 2 МПа и температуре 273 К
4.2.72 На рисунке показан график процесса, происходящего с идеальным газом. Укажите точки
4.2.73 На PT-диаграмме изображен замкнутый процесс, который совершает кислород некоторой
4.2.74 Если нагреть 1 моль идеального газа на 1 К при постоянном объеме, то давление возрастет
4.2.75 Имеется два сосуда с одним и тем же газом при одинаковой температуре. Плотность газа
4.2.76 При увеличении температуры газа на 60 К его объем возрос на 1 л. На сколько литров
4.2.77 Насос захватывает при каждом качании 1 л воздуха при нормальных условиях и нагнетает
4.2.78 Воздушный шар имеет легкорастяжимую теплоизолированную оболочку массой 130 кг
4.2.79 В некотором процессе давление и объем идеального газа связаны соотношением
4.2.80 Какой радиус должен иметь наполненный гелием воздушный шар, чтобы он мог подняться
4.2.81 Надувной шарик, заполненный гелием, удерживают на нити. Найдите натяжение нити
4.2.82 Два баллона с объемами 20 и 10 л соединены длинной тонкой трубкой и содержат 6 моль
4.2.83 Воздушный шар объемом 20 м3, наполненный гелием, поднялся на высоту 180 м за 0,5 минуты
4.2.84 Внутри замкнутого цилиндра, наполненного воздухом, находится шарик радиусом 3 см
4.2.85 На дне цилиндра, наполненного воздухом, плотность которого 1,29 кг/м3, лежит полый
4.2.86 В замкнутом сосуде к верхней стенке на пружине жесткостью 4 Н/м подвешена сфера
4.2.87 Во сколько раз изменится температура идеального газа, если уменьшить его объем
4.2.88 Внутри закрытого с обоих концов горизонтального цилиндра есть поршень
4.2.89 Тонкий резиновый шар радиусом 2 см наполнен воздухом при температуре 20 C
4.2.90 Цилиндрический сосуд делится невесомым поршнем на две части. В одну часть сосуда
4.2.91 Два одинаковых шара соединены тонкой трубкой, в которой находится капелька ртути
4.2.92 Внутри закрытого с обоих концов горизонтального цилиндра имеется тонкий поршень
4.2.93 Два одинаковых сосуда, содержащих газ при 300 К, соединили горизонтальной трубкой
4.2.94 Горизонтально расположенный цилиндр разделен скользящей без трения перегородкой
4.2.95 Объем пузырька, всплывающего на поверхность со дна озера, увеличился в два раза
4.2.96 Состояние одного киломоля идеального газа менялось по графику 1-2-3. Определить
4.2.97 Сосуд объемом 5 л разделен перегородкой на две части, заполненные одним газом
4.2.98 При некотором процессе идеального газа связь между давлением и объемом газа pV^3=const
4.2.99 Воздушный шар объемом 1000 м3 наполнен гелием при температуре окружающего воздуха
4.2.100 В цилиндре с площадью основания 100 см2 находится воздух. Поршень расположен на высоте
4.2.101 В сосуд, на дне которого лежит твердый шар, нагнетают воздух при температуре 27 C
4.2.102 В закрытом с обоих концов цилиндре длиной 2 м поршень соединён с днищами пружинами
4.2.103 Тонкостенный резиновый шар собственным весом 0,6 Н наполнен неоном и погружен в озеро
4.2.104 Давление воздуха в сосуде равно 102,4 кПа. Вместимость цилиндра разрежающего насоса
4.2.105 Компрессор всасывает в 1 мин 3 м3 сухого воздуха при температуре 290 К и давлении 100 кПа
4.2.106 Давление воздуха в сосуде 97 кПа. После трёх ходов откачивающего поршневого насоса
4.2.107 В цилиндре длиной 2L=2 м тонкий поршень соединён с днищами пружинами одинаковой
4.2.108 Газ, занимающий при температуре 127 C и давлении 100 кПа объем 2 л, изотермически
4.2.109 В цилиндре под поршнем находится газ при нормальных условиях. Сначала объем газа
4.2.110 При увеличении абсолютной температуры идеального газа в 2 раза его давление
4.2.111 Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%
Изопроцессы
4.3.1 Определить начальную температуру газа, если при изохорном нагревании
4.3.2 В закрытом баллоне находится газ при температуре 295 К
4.3.3 Давление в откачанной рентгеновской трубке при 15 градусах Цельсия
4.3.4 На сколько Кельвин надо нагреть воздух при постоянном давлении
4.3.5 Газ изотермически сжимают от объема 0,15 м3 до объема 0,1 м3
4.3.6 Газ нагрели на 1 К при постоянном объеме. Давление газа при этом
4.3.7 Газ нагрели на 100 К при постоянном объеме. Давление газа
4.3.8 В закрытом сосуде находится идеальный газ. Во сколько раз
4.3.9 Во сколько раз изменяется плотность идеального газа
4.3.10 В процессе изобарного нагревания газа его объем увеличился в 2 раза
4.3.11 Сосуд объемом 12 м3, содержащий газ под давлением 400 кПа
4.3.12 Сосуд, содержащий 10 л воздуха при давлении 1 МПа, соединяют с пустым
4.3.13 Резиновая камера содержит воздух под давлением 104 кПа. Камеру
4.3.14 До какой температуры нужно нагреть воздух, взятый при 20 градусах
4.3.15 Объем некоторой массы газа при изобарном нагревании на 10 К
4.3.16 Даны две изохоры для одной и той же массы идеального газа
4.3.17 Газ сжат изотермически от 8 до 6 л. Давление при этом возросло
4.3.18 В сосуде объемом 1 л при температуре 183 градуса Цельсия находится
4.3.19 В цилиндре под поршнем изотермически сжимают 9 г водяного
4.3.20 Во сколько раз изменится плотность идеального газа при температуре
4.3.21 При 27 градусах Цельсия газ занимает объем 10 л. До какой
4.3.22 Продукты сгорания газа охлаждаются в газоходе с 1000 до 300 градусов
4.3.23 Газ занимает объем 8 л при температуре 300 К. Определите массу газа
4.3.24 Давление азота в электрической лампочке объемом 0,15 л равно 68 кПа
4.3.25 Бутылка с газом закрыта пробкой, площадь сечения которой 2,5 см2
4.3.26 В цилиндре под поршнем находится газ. Масса поршня 0,6 кг
4.3.27 Два сосуда объемом 2 и 4 л, заполненные одинаковым газом, соединены
4.3.28 В цилиндре под поршнем находится воздух. Вес поршня 60 Н
4.3.29 В цилиндре под поршнем находится вода массой 35 мг и пар массой 25 мг
4.3.30 Баллон, наполненный воздухом при температуре 273 К и атмосферном
4.3.31 В цилиндре под поршнем находится воздух при давлении 0,2 МПа
4.3.32 Один конец цилиндрической трубки, длина которой 25 см и радиус 1 см
4.3.33 Расположенная горизонтально, запаянная с обоих концов стеклянная трубка
4.3.34 В вертикальном закрытом цилиндре находится подвижный поршень
4.3.35 Открытую стеклянную трубку длиной 1 м наполовину погружают в ртуть
4.3.36 В стеклянной трубке находится столбик ртути длиной 10 см. Когда
4.3.37 Посередине откачанной и запаянной с обоих сторон горизонтально
4.3.38 Открытую с обеих сторон стеклянную трубку длиной 60 см
4.3.39 В трубке длиной 1,73 м, заполненной газом, находится столбик ртути
4.3.40 В каком из изображенных на рисунке процессов, проведенных
4.3.41 Горизонтально расположенный закрытый цилиндрический сосуд
4.3.42 На рисунке изображены гиперболы для трех идеальных газов с одинаковыми массами
4.3.43 На рисунке изображены гиперболы для трех идеальных газов с разными массами
4.3.44 Постоянную массу идеального газа переводят из состояния 1
4.3.45 Горизонтально расположенный закрытый цилиндрический сосуд длины
4.3.46 Температура воздуха в комнате повысилась от 17 до 27 градусов Цельсия
4.3.47 Газ при 27 градусах Цельсия занимает объем V. До какой температуры
4.3.48 Баллон, содержащий 12 л кислорода при давлении 1 МПа, соединяют
Влажность
4.4.1 Определите относительную влажность воздуха при температуре 18 C, если точка росы
4.4.2 Определите давление водяных паров в воздухе при температуре 20 С и относительной
4.4.3 5 м3 воздуха при температуре 25 С содержат 86,5 г водяного пара. Определить абсолютную
4.4.4 Определить абсолютную влажность воздуха при температуре 37 C, если давление
4.4.5 В 6 м3 воздуха с температурой 19 С содержится 51,3 г водяного пара. Определите
4.4.6 В 10 м3 воздуха с температурой 19 С содержится 71,3 г водяного пара. Определите
4.4.7 В комнате объемом 120 м3 при температуре 15 C относительная влажность составляет 60%
4.4.8 Найти массу водяного пара, содержащегося в спортивном зале объемом 1100 м3
4.4.9 В комнате объемом 200 м3 относительная влажность воздуха при 20 С равна 70%
4.4.10 При температуре 22 C относительная влажность воздуха равна 60%. Найти относительную
4.4.11 В комнате размером 10x5x3 м3 поддерживается температура 293 К, а точка росы 283 К
4.4.12 В цистерне объемом 10 м3 находится воздух с относительной влажностью 70%
4.4.13 Воздух в помещении имеет температуру 24 C и относительную влажность 50%. Определите
4.4.14 Найти массу водяных паров в 1 м3 воздуха при нормальном атмосферном давлении
4.4.15 Давление водяного пара в воздухе на 40% ниже давления насыщенных паров при этой же
4.4.16 В сосуде объемом 100 л при 27 C находится воздух с относительной влажностью 30%
4.4.17 Влажность в комнате объемом 520 м3 при температуре 25 C равна 90%. Какое количество
4.4.18 Сколько надо испарить воды в 1000 м3 воздуха, относительная влажность которого 40%
4.4.19 В комнате объемом 60 м3 при температуре 18 C относительная влажность воздуха 50%
( 63 оценки, среднее 4.44 из 5 )
8. Молекулярно-кинетическая теория
1. Вспоминай формулы по каждой теме
2. Решай новые задачи каждый день
3. Вдумчиво разбирай решения
Основы МКТ
При давлении (p_o) =10(^6) Па идеальный газ занимает объём (V_o = 5) л. В результате изотермического расширения его объём увеличился на (Delta V = 1) л, а концентрация молекул стала равна (n=3,62cdot10^{26}) м(^{-3}). При какой температуре проводился опыт? (Ответ дайте в кельвинах и округлите до целого числа.)
Так как процесс изотермический, то по закону Бойля-Мариотта: [p_oV_o=p_1V_1hspace{5 mm} (1)] Так как объем газа увеличился на (Delta V), то: [V_1=V_o+Delta V hspace{5 mm} (2)] Подставим (2) в (1) и выразим конечное давление (p_1): [p_1=dfrac{p_oV_o}{V_o+Delta V}] В то же время конечное давление равно: [p_1=nkT] где (k) — постоянная Больцмана. Выразим отсюда температуру, при которой проводился опыт: [T=dfrac{p_1}{nk}=dfrac{p_0V_0}{(V_0+Delta V)nk}] Переведем значения величин в СИ и подставим их в формулу: [T=dfrac{10^6text{ Па}cdot5cdot10^{-3}text{ м}^3}{6cdot10^{-3}text{ м}^3cdot3,62cdot10^{26}text{ м}^{-3}cdot1,38cdot10^{-23}text{ Дж/К}}approx 167 text{ К}]
Ответ: 167
Абсолютную температуру идеального газа уменьшили в 4 раза. Во сколько раз уменьшится средняя квадратичная скорость теплового движения молекул этого газа?
Средняя кинетическая энергия вычисляется по формуле: [E_{k}=dfrac{3}{2}kT] где (k) — постоянная Больцмана, (T) — абсолютная температура газа.
В свою очередь кинетическая энергия равна: [dfrac{m_o v^2}{2}=dfrac{3}{2}kT] где (m_o) — масса одной молекулы, (v) — средняя квадратичная скорость теплового движения.
Отсюда получим зависимость: [v^2sim T] [vsim sqrt{T}] При уменьшении абсолютной температуры идеального газа в 4 раза средняя квадратичная скорость теплового движения уменьшится в 2 раза.
Ответ: 2
В результате нагревания газа средняя кинетическая энергия теплового движения его молекул увеличилась в 4 раза. Во сколько раз увеличилась при этом абсолютная температура газа?
Средняя кинетическая энергия вычисляется по формуле: [E_k=dfrac{3}{2}kT] где (k) — постоянная Больцмана, (T) — абсолютная температура газа.
При увеличении энергии в 4 раза, температура увеличится в 4 раза.
Ответ: 4
В сосуде находится смесь двух газов: кислорода и водорода. Число молекул кислорода в сосуде равно (4 cdot10^{23}), а молекул водорода — (32 cdot 10^{23}). Чему равно отношение (dfrac{nu_{O_{2}} }{nu_{H_{2}}}) количеств веществ этих газов?
Количество вещества можно найти по формуле: [nu=dfrac{N}{N_A}] где (N) — число молекул газа, (N_A) — число Аводгадро.
Искомое отношение равно: [dfrac{nu_{O_{2}}}{nu_{H_{2}}}=dfrac{N_1}{N_2}] где (N_1) и (N_2) — число молекул кислорода и водорода соответственно. [dfrac{nu_{O_{2}}}{nu_{H_{2}}}=dfrac{4cdot10^{23}}{32cdot10^{23}}=0,125]
Ответ: 0,125
Во сколько раз число молекул кислорода отличается от числа атомов меди при нормальных условиях, если (mu(O_2)= 0,032) кг/моль, (mu(Cu) = 0,064) кг/моль, а количество вещества как меди, так и кислорода равно 3 моль?
Количество вещества можно найти по формуле: [nu=dfrac{N}{N_A}] где (N)—число молекул газа, (N_A) — число Авогадро. Выразим отсюда число атомов/молекул: [N = nu N_A] Найдем отношение числа молекул кислорода к числу атмов меди: [dfrac{N_{O_{2}}}{N_{Cu}} = dfrac{nu_{O_{2}}N_A}{nu_{Cu} N_A}] Так как по условию (nu_{Cu} = nu_{O_{2}}), то: [dfrac{N_{O_{2}}}{N_{Cu}} =1]
Ответ: 1
В баллоне находится 3(cdot10^{23}) молекул газа. Какое примерно количество вещества находится в баллоне? (Ответ дайте в молях.)
Количество вещества находится по формуле: [nu=dfrac{N}{N_A}] где (N) — число молекул газа, (N_A) — число Авогадро. [nu=dfrac{3cdot10^{23}}{6cdot10^{23}text{ моль}^{-1}}=0,5 text{ моль}]
Ответ: 0,5
Средняя кинетическая энергия хаотического теплового движения молекул гелия уменьшилась в 4 раза. Определите конечную температуру газа, если его начальная температура равна 1000 К. Ответ дайте в кельвинах.
Связь средней кинетической энергии и температуры выражена в формуле: [E_k=dfrac{3}{2}kT] где (k) — постоянная Больцмана.
Так как энергия уменьшилась в 4 раза, то и температура гелия уменьшится в 4 раза. [T_1=dfrac{T_o}{4}=frac{1000text{ К}}{4}=250 text{ К}]
Ответ: 250

Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Курс Глицин. Любовь, друзья, спорт и подготовка к ЕГЭ
Инфоурок
›
Физика
›Презентации›Подготовка к ЕГЭ по физике. Решение задач на тему «МКТ и газовые законы»
Подготовка к ЕГЭ по физике. Решение задач на тему «МКТ и газовые законы»
Скачать материал

Скачать материал


- Сейчас обучается 140 человек из 50 регионов


- Сейчас обучается 46 человек из 28 регионов


- Сейчас обучается 31 человек из 20 регионов


Описание презентации по отдельным слайдам:
-
1 слайд
РЕШЕНИЕ ЗАДАЧ ПО ТЕМЕ «Молекулярно-кинетическая теория»
(подготовка к ЕГЭ по физике, 11 класс)
Учитель физики МБОУ «Обоянская СОШ №2»
Мазуркевич Наталья Вячеславовна -
2 слайд
ОТВЕТЬТЕ НА ВОПРОСЫ
Перечислите три утверждения. Которые лежат в основе молекулярно-кинетической теории строения вещества
Что нам известно о строении газообразных, жидких и твёрдых тел? -
3 слайд
ОТВЕТЬТЕ НА ВОПРОСЫ
Что характеризует температура?
Какой газ называется идеальным?
Что называют тепловым равновесием?
Какие макроскопические параметры вам известны? -
4 слайд
ОТВЕТЬТЕ НА ВОПРОСЫ
Перечислите газовые законы, известные вам.
Какой пар называется насыщенным?
Какие формулы МКТ вам известны? -
-
-
7 слайд
Выбери правильный ответ
Одним из подтверждений положения молекулярно-кинетической теории строения вещества о том, что частицы вещества хаотично движутся, может служить:A. Возможность испарения жидкости при любой температуре.
Б. Зависимость давления столба жидкости от глубины.
B. Выталкивание из жидкости погруженных в нее тел. -
8 слайд
Выбери правильный ответ
Идеальный газ, находящийся в закрытом сосуде, оказывает давление на его стенки. Это объясняется тем что1) молекулы прилипают к стенкам сосуда;
2) идеальный газ имеет большую плотность;
3) молекулы газа передают стенкам энергию;
4) молекулы газа передают стенкам импульс. -
9 слайд
Выбери правильный ответ
Выберите неверное утверждение:1) все вещества состоят из частиц;
2) между всеми частицами действуют гравитационные силы;
3) в любом агрегатном состоянии вещество не является сплошным;
4) силы притяжения между частицами вещества всегда меньше сил отталкивания. -
10 слайд
Выбери правильный ответ
Аморфными называют тела,1) атомная структура которых имеет ближний порядок и не имеет дальнего порядка;
2) которые находятся в твёрдом состоянии и представляют собой один большой кристалл;
3) которые находятся в твёрдом состоянии и состоят из большого числа хаотически расположенных мелких кристаллов;
4) которые находятся в жидком состоянии; -
11 слайд
Выбери правильный ответ
Дима и Лена схематически изобразили на доске сосуд, в котором находится идеальный газ.Отвечающим модели броуновского движения можно признать рисунок, сделанный А) Димой Б) Леной
1) только А;
2) только Б;
3) и А, и Б;
4) ни А, ни Б. -
12 слайд
Задача №1
В 4 м. куб. воздуха при температуре 289К находится 40г водяного пара. Найти относительную влажность воздуха, если Ро=1, 81 кПа. -
13 слайд
Задача №2
Какова средняя квадратичная скорость движения молекул газа, если имея массу 6 кг, он занимает объём 5метров куб. при давлении 200кПа? -
14 слайд
Задача №3
Определите среднюю кинетическую энергию молекулы одноатмного газа и концентрацию молекул при давлении 0,8 МПа и температуре 17 градусов по Цельсию? -
15 слайд
Задача №4
Каково давление сжатого воздуха, находящегося в баллоне вместимостью 20л при 12 градусах по Цельсию, если масса этого воздуха 2 кг? -
16 слайд
Задача №5
Сколько молекул содержится в 2г водорода?
-
17 слайд
Задача №6
1. Назовите каждый цикл процесса
2. Изобразите этот процесс в координатах РТ -
18 слайд
Задача №7
В баллоне вместимостью 25л находится смесь газов, состоящая из аргона массой 20г и гелия массой 2г при температуре 301К. Найти давление смеси газов на стенки сосудов. -
19 слайд
ДОМАШНЕЕ ЗАДАНИЕ
1. Портал РЕШУ ЕГЭ. Каталог заданий.
Качественные задачи и основные положения МКТ
2. Смесь одинаковых масс гелия, водорода и азота помещена в сосуд и нагрета до температуры 350К. Плотность смеси оказалась равной 50г/м.куб. Чему равно давление в сосуде? -
20 слайд
СПАСИБО ЗА РАБОТУ
Краткое описание документа:
В данной презентации рассмотрены задачи по физике 10 класса на знание законов МКТ и газовых законов. Слайды сопровождаются рисунками, тестами, вопросами с выбором правильного ответа. Даётся материал на повторение законов и формул.Материал презентации соответствует ФГОС. В конце даётся домашнее задание: задачи на закрепление темы «МКТ и газовые законы»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
6 153 785 материалов в базе
- Выберите категорию:
- Выберите учебник и тему
- Выберите класс:
-
Тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
-
Найти материалы
Другие материалы
- 25.03.2019
- 410
- 0

- 25.03.2019
- 1732
- 57
- 25.03.2019
- 358
- 0




- 24.03.2019
- 2199
- 50

Вам будут интересны эти курсы:
-
Курс повышения квалификации «Информационные технологии в деятельности учителя физики»
-
Курс профессиональной переподготовки «Организация и предоставление туристских услуг»
-
Курс повышения квалификации «Экономика и право: налоги и налогообложение»
-
Курс повышения квалификации «Специфика преподавания конституционного права с учетом реализации ФГОС»
-
Курс профессиональной переподготовки «Организация деятельности по подбору и оценке персонала (рекрутинг)»
-
Курс повышения квалификации «Правовое регулирование рекламной и PR-деятельности»
-
Курс повышения квалификации «ЕГЭ по физике: методика решения задач»
-
Курс профессиональной переподготовки «Политология: взаимодействие с органами государственной власти и управления, негосударственными и международными организациями»
-
Курс профессиональной переподготовки «Методика организации, руководства и координации музейной деятельности»
-
Курс профессиональной переподготовки «Гостиничный менеджмент: организация управления текущей деятельностью»
-
Курс профессиональной переподготовки «Стандартизация и метрология»
-
Настоящий материал опубликован пользователем Мазуркевич Наталья Вячеславовна. Инфоурок является
информационным посредником и предоставляет пользователям возможность размещать на сайте
методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них
сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайтЕсли Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.Удалить материал
-
- На сайте: 5 лет и 4 месяца
- Подписчики: 0
- Всего просмотров: 159116
-
Всего материалов:
63
Любишь теорию – люби и задачи решать. Во всяком случае, лучше полюбить, ведь заниматься этим все равно придется. Сегодня занимаемся решением задач по молекулярно-кинетической теории и радуемся.
Присоединяйтесь к нам в телеграм и будьте в курсе самых актуальных студенческих новостей.
А прежде чем приступать к решению задач, вспомните памятку по решению задач по физике и держите наготове основные формулы.
Задачи по молекулярно-кинетической теории
Задача №1. Средняя квадратичная скорость молекул и температура
Условие
При какой температуре средняя квадратичная скорость молекул кислорода больше их наиболее вероятной скорости на 100 м/с.
Решение
Находим разницу скоростей, используя формулы для средней квадратичной и наиболее вероятной скорости молекул:
Отсюда выражаем температуру:
Ответ: 121 К.
Задача №2. Изопроцессы
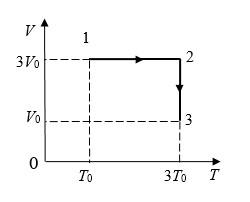
Условие
На диаграмме V – T изображены процессы перехода идеального газа постоянного количества из состояния 1 в состояние 3. Каким соотношением связаны конечное давление Р3 и начальное давление Р1?
Решение
При изохорном процессе:
Далее при изотермическом:
Ответ: Р3=9Р1
Задача №3. Приращение энтропии
Условие
Найти приращение энтропии при переходе массы m=8 г углекислого газа от объема V1=10 л при температуре t1=80° С к объему V2=40 л при температуре t2=300° С.
Решение
Рассмотрим процесс перехода между состояниями вначале по
изохоре, а затем по изотерме:
Соответствующие изменения при каждом процессе:
В сумме получаем общее изменение энтропии:
Ответ: 3,9 Дж/К.
Задача №4. Молярная масса
Условие
Каковы масса и молярная масса одной молекулы воды.
Решение
Молекула воды состоит из двух атомов водорода и одного атома кислорода. Их относительные атомные массы берем в таблице Менделеева, а затем вычисляем относительную молярную массу молекулы:
Молярная масса воды:
Чтобы найти массу одной молекулы, разделим массу моля воды на количество молекул, содержащихся в нем (число Авогадро):
Ответ: 3*10^-26 кг.
Задача №5. Основное уравнение молекулярно-кинетической теории
Условие
Каково давление газа на стенки сосуда, если известны средний квадрат скорости его молекул (2*10^6 м2/с2), концентрация молекул (4*10^24 1/м^3) и масса одной молекулы (3*10^-25 кг).
Решение
Используем основное уравнение МКТ:
Ответ: 800 кПа.
Вопросы по молекулярно кинетической теории
Вопрос 1. Что такое основное уравнение МКТ?
Ответ. Основное уравнение МКТ – это уравнение, которое связывает макроскопические параметры системы (давление, объем, температура) с микроскопическими (масса молекул, скорость движения молекул)
Вопрос 2. Сформулируйте основные положения МКТ.
Ответ. Основные положения молекулярно-кинетической теории:
- Все вещества могут быть в жидком, твердом и газообразном состоянии. Вещество состоит из частиц (молекулы, атомы, ионы). Элементарные молекулы могут иметь сложное строение, то есть иметь в своем составе несколько атомов. Молекулы и атомы – электрически нейтральные частицы, которые в определенных условиях приобретают дополнительный электрический заряд и переходят в положительные или отрицательные ионы.
- Частицы вещества постоянно находятся в хаотическом движении.
- Силы, с которыми частицы взаимодействуют между собой, имеют электрическую природу. Гравитационным взаимодействием между частицами можно пренебречь.
Вопрос 3. Что такое 1 моль вещества?
Ответ. Это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0,012 кг углерода.
Вопрос 4. Каково экспериментальные подтверждение хаотического движения молекул?
Ответ. Броуновское движение – наиболее очевидное подтверждение второго положения МКТ.
Броуновское движение – это тепловое хаотическое движение микроскопических частиц, взвешенных в жидкости или газе.
Было открыто ботаником Робертом Броуном в 1827 году на примере пыльцы, но первые сведения об описании подобных явлений относятся к Древнему Риму.
Вопрос 5. Что происходит с кинетической энергией теплового движения молекул при спаде температуры.
Ответ. С ростом температуры кинетическая энергия теплового движения увеличивается, а при спаде температуры – наоборот, уменьшается.
В 19 веке существовала гипотеза тепловой смерти Вселенной, согласно которой в определенный момент, при достижении абсолютного нуля температуры, все процессы остановятся, и Вселенная придет в состояние термодинамического равновесия. В настоящее время эта теория опровергнута.
Нужна помощь в решении задач и других заданий по учебе? Профессиональный студенческий сервис и его лучшие специалисты всегда к вашим услугам и справятся с любой темой.