Тренировочные упражнения по теме «Гидролиз солей. Среда водных растворов» в формате ЕГЭ по химии (тренажер задания 21 ЕГЭ по химии).
Внимание! Перед выполнением тестов я рекомендую внимательно изучить теорию по теме «Гидролиз» (теория для решения задания 21 ЕГЭ по химии).
Для выполнения задания 21 используйте следующие справочные данные.
Тренировочный тест «Гидролиз солей. Среда водных растворов» 10 вопросов, при каждом прохождении новые.
181
Создан на
16 января, 2022 От Admin
Тренажер задания 21
Тренажер задания 21 ЕГЭ по химии
1 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KNO2
2) LiOH
3) ZnSO4
4) Ba(NO3)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
2 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) Na3PO4
2) NH4Br
3) (CH3COO)2Cu
4) HClO3
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
3 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сульфат железа
2) нитрат бария
3) сульфид натрия
4) азотная кислота
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
4 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S
2) Na3PO4
3) HNO3
4) LiCl
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
5 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4
2) Fe(NO3)3
3) K2SO3
4) HClO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
6 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) уксусная кислота
2) метиламин
3) азотная кислота
4) гидроксид кальция
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
7 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (CH3COO)2Ca
2) HNO3
3) NH4ClO4
4) LiOH
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
8 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) силикат натрия
2) фосфорная кислота
3) нитрат кальция
4) гидроксид бария
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
9 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3
2) BaBr2
3) KOH
4) FeCl3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
10 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HNO2
2) C2H5COOK
3) H2CrO4
4) Ca(OH)2
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
Ваша оценка
The average score is 26%
Полный тематический тест по теме «Гидролиз солей. Среда водных растворов» — полный тест из всех вопросов.
31
Создан на
03 апреля, 2022 От Admin
Полный тематический тест Тренажер задания 21
Тренажер задания 21 ЕГЭ по химии
1 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) K2CO3
2) Cu(NO3)2
3) Li2SO4
4) НClO4
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
2 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) KOH
2) NaHCO3
3) H3PO4
4) НCl
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
3 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) NaHSO4
2) KClO4
3) CH3COOH
4) KHCO3
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
4 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) Na3PO4
2) NH4Br
3) (CH3COO)2Cu
4) HClO3
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
5 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HNO2
2) C2H5COOK
3) H2CrO4
4) Ca(OH)2
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
6 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HI
2) H2S
3) Na2Cr2O7
4) KNO2
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
7 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HIO3
2) Li2S
3) NaClO4
4) NH4NO3
Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
8 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) LiIO3
2) HMnO4
3) Ca(HS)2
4) Mg(ClO4)2
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
9 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HF
2) HI
3) CaCrO4
4) Cs3PO4
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
10 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H3РО4
2) Nа3РО4
3) NaNO3
4) Ba(ОН)2
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
11 / 58
Для веществ, приведённых в. перечне, определите характер среды их водных растворов.
1) H2S
2) NaNO2
3) Ca(NO3)2
4) НВr
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
12 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HCOOH
2) CH3COOK
3) Sr(OH)2
4) KI
Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
13 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (NH4)2SO4
2) NH3
3) CsOH
4) HClO3
Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
14 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Аl(NO3)3
2) NH3
3) CH3COONH4
4) HClO3
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
15 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3COOH
2) К3РО4
3) НNO3
4) LiOH
Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
16 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3NH2
2) KClO4
3) Аl(NO3)3
4) Ba(OH)2
Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
17 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaClO3
2) KClO
3) (NH4)2SO4
4) HI
Запишите номера веществ в порядке убывания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
18 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4NO3
2) CH3COOK
3) BaCl2
4) RbOH
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
19 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Cr(NO3)3
2) Ca(OH)2
3) CH3COONH4
4) HClO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
20 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) силикат натрия
2) фосфорная кислота
3) нитрат кальция
4) гидроксид бария
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
21 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сероводород
2) аммиак
3) бромоводород
4) нитрат бария
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
22 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) ацетат кальция
2) перхлорат калия
3) гидроксид стронция
4) метановая кислота
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
23 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) хлорид аммония
2) бромоводород
3) гидроксид цезия
4) силикат калия
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
24 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сульфат железа
2) нитрат бария
3) сульфид натрия
4) азотная кислота
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
25 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S
2) Na3PO4
3) HNO3
4) LiCl
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
26 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) C6H5OK
2) NaClO4
3) Cr(NO3)3
4) Sr(OH)2
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
27 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Рb(NO3)2
2) Ca(ClO)2
3) NaI
4) KOH
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
28 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сульфат аммония
2) ацетат калия
3) нитрат бария
4) гидроксид калия
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
29 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сероводород
2) иодоводород
3) сульфат лития
4) карбонат рубидия
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
30 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) бромид хрома(III)
2) ацетат калия
3) иодоводород
4) нитрат лития
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
31 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) уксусная кислота
2) метиламин
3) азотная кислота
4) гидроксид кальция
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
32 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4Br
2) HI
3) Na2SiO3
4) KClO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
33 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3
2) Н3РО4
3) Ва(NO3)2
4) Са(ОН)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
34 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S
2) CH3COONH4
3) CH3NH2
4) HClO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
35 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (НСOO)2Са
2) KClO4
3) Sr(OH)2
4) HCOOH
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
36 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4NO3
2) HNO3
3) Na2S
4) K2SO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
37 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Fе2(SO4)3
2) LiNO3
3) K2SiO3
4) H2SO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
38 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) FeBr3
2) НСООNa
3) НВr
4) LiOH
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
39 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaF
2) RbOH
3) HCl
4) СаBr2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
40 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3COOK
2) SrCl2
3) FeCl2
4) HNO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
41 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KHCO3
2) Ba(NO3)2
3) ZnSO4
4) HCIO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
42 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2SO4
2) Na2S
3) AICl3
4) CaCl2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
43 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3
2) BaBr2
3) KOH
4) FeCl3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
44 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (CH3COO)2Ca
2) HNO3
3) NH4ClO4
4) LiOH
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
45 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2SO4
2) AI(NO3)3
3) KOH
4) K2CO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
46 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4
2) Fe(NO3)2
3) K2SO3
4) HCIO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
47 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HBr
2) Cu(NO3)2
3) Na2SO4
4) KHCO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
48 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H3PO4
2) Na2CO3
3) K2SO4
4) AICl3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
49 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) FeCl2
2) HNO3
3) K3PO4
4) LiOH
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
50 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4
2) Fe(NO3)3
3) K2SO3
4) HClO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
51 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KF
2) LiNO3
3) (NH4)2SО4
4) H2SО4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
52 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KCI
2) CrCl2
3) HI
4) K2S
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
53 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) K2SО3
2) ZnSO4
3) Ba(NO3)2
4) Ca(OH)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
54 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KNO2
2) LiOH
3) ZnSO4
4) Ba(NO3)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
55 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HF
2) NH3
3) (NH4)2SO4
4) Sr(OH)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
56 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CuSO4
2) NaOH
3) K2SO3
4) Ca(NO3)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
57 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3
2) ZnCl2
3) K2SO4
4) HBr
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
58 / 58
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaClO4
2) FeCl3
3) HClO4
4) KHCO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
Ваша оценка
The average score is 29%
| Задание 1 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) K2CO3 2) Cu(NO3)2 3) Li2SO4 4) НClO4 Запишите номера веществ в порядке возрастания значения pH их водных растворов. |
Решение:
НClO4 — сильная кислота, диссоциирует в растворе практически полностью:
НClO4 = Н+ + ClO4—
Среда водного раствора НClO4 — кислая, рН намного меньше 7
K2CO3 — соль, образованная сильным основанием KOH и слабой кислотой H2CO3
Гидролизуется по аниону:
CO32- + H2O = НCO3— + OH—
Среда водного раствора K2CO3 — слабощелочная, рН немного выше 7
Cu(NO3)2 — соль, образованная слабым основанием Cu(OH)2 и сильной кислотой HNO3
Гидролизуется по катиону:
Cu2+ + H2O = CuOH+ + H+
Среда водного раствора Cu(NO3)2 — слабокислая, рН немного ниже 7
Li2SO4 — соль, образованная сильным основанием LiOH и сильной кислотой H2SO4
Гидролизу не подвергается, среда водного раствора нейтральная, рН примерно равен 7.
Ответ: 4231
| Задание 2 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) KOH 2) NaHCO3 3) H3PO4 4) НCl Запишите номера веществ в порядке уменьшения значения pH их водных растворов. |
| Задание 3 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) NaHSO4 2) KClO4 3) CH3COOH 4) KHCO3 Запишите номера веществ в порядке возрастания значения pH их водных растворов. |
| Задание 4 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) Na3PO4 2) NH4Br 3) (CH3COO)2Cu 4) HClO3 Запишите номера веществ в порядке уменьшения значения pH их водных растворов. |
| Задание 5 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HNO2 2) C2H5COOK 3) H2CrO4 4) Ca(OH)2 Запишите номера веществ в порядке уменьшения значения pH их водных растворов. |
| Задание 6 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HI 2) H2S 3) Na2Cr2O7 4) KNO2 Запишите номера веществ в порядке возрастания значения pH их водных растворов. |
| Задание 7 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HIO3 2) Li2S 3) NaClO4 4) NH4NO3 Запишите номера веществ в порядке уменьшения значения pH их водных растворов. |
| Задание 8 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) LiIO3 2) HMnO4 3) Ca(HS)2 4) Mg(ClO4)2 Запишите номера веществ в порядке возрастания значения pH их водных растворов. |
| Задание 9 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) HF 2) HI 3) CaCrO4 4) Cs3PO4 Запишите номера веществ в порядке возрастания значения pH их водных растворов. |
| Задание 10 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H3РО4 2) Nа3РО4 3) NaNO3 4) Ba(ОН)2 Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 11 | |
| Для веществ, приведённых в. перечне, определите характер среды их водных растворов.
1) H2S 2) NaNO2 3) Ca(NO3)2 4) НВr Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 12 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HCOOH 2) CH3COOK 3) Sr(OH)2 4) KI Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 13 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (NH4)2SO4 2) NH3 3) CsOH 4) HClO3 Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 14 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Аl(NO3)3 2) NH3 3) CH3COONH4 4) HClO3 Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 15 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3COOH 2) К3РО4 3) НNO3 4) LiOH Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 16 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3NH2 2) KClO4 3) Аl(NO3)3 4) Ba(OH)2 Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 17 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaClO3 2) KClO 3) (NH4)2SO4 4) HI Запишите номера веществ в порядке убывания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 18 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4NO3 2) CH3COOK 3) BaCl2 4) RbOH Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 19 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Cr(NO3)3 2) Ca(OH)2 3) CH3COONH4 4) HClO4 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 20 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) силикат натрия 2) фосфорная кислота 3) нитрат кальция 4) гидроксид бария Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 21 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сероводород 2) аммиак 3) бромоводород 4) нитрат бария Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 22 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) ацетат кальция 2) перхлорат калия 3) гидроксид стронция 4) метановая кислота Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 23 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) хлорид аммония 2) бромоводород 3) гидроксид цезия 4) силикат калия Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 24 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сульфат железа 2) нитрат бария 3) сульфид натрия 4) азотная кислота Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 25 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S 2) Na3PO4 3) HNO3 4) LiCl Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 26 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) C6H5OK 2) NaClO4 3) Cr(NO3)3 4) Sr(OH)2 Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 27 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Рb(NO3)2 2) Ca(ClO)2 3) NaI 4) KOH Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 28 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сульфат аммония 2) ацетат калия 3) нитрат бария 4) гидроксид калия Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 29 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) сероводород 2) иодоводород 3) сульфат лития 4) карбонат рубидия Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 30 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) бромид хрома(III) 2) ацетат калия 3) иодоводород 4) нитрат лития Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 31 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) уксусная кислота 2) метиламин 3) азотная кислота 4) гидроксид кальция Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 32 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4Br 2) HI 3) Na2SiO3 4) KClO4 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 33 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3 2) Н3РО4 3) Ва(NO3)2 4) Са(ОН)2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 34 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2S 2) CH3COONH4 3) CH3NH2 4) HClO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 35 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (НСOO)2Са 2) KClO4 3) Sr(OH)2 4) HCOOH Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 36 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4NO3 2) HNO3 3) Na2S 4) K2SO4 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 37 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Fе2(SO4)3 2) LiNO3 3) K2SiO3 4) H2SO4 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 38 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) FeBr3 2) НСООNa 3) НВr 4) LiOH Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 39 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaF 2) RbOH 3) HCl 4) СаBr2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая. |
| Задание 40 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3COOK 2) SrCl2 3) FeCl2 4) HNO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 41 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KHCO3 2) Ba(NO3)2 3) ZnSO4 4) HCIO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 42 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2SO4 2) Na2S 3) AICl3 4) CaCl2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 43 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3 2) BaBr2 3) KOH 4) FeCl3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 44 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H3PO4 2) Na2CO3 3) K2SO4 4) AICl3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 45 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HBr 2) Cu(NO3)2 3) Na2SO4 4) KHCO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 46 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4 2) Fe(NO3)2 3) K2SO3 4) HCIO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 47 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) H2SO4 2) AI(NO3)3 3) KOH 4) K2CO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 48 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) (CH3COO)2Ca 2) HNO3 3) NH4ClO4 4) LiOH Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 49 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) K2SО3 2) ZnSO4 3) Ba(NO3)2 4) Ca(OH)2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 50 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KCI 2) CrCl2 3) HI 4) K2S Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 51 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KF 2) LiNO3 3) (NH4)2SО4 4) H2SО4 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 52 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4 2) Fe(NO3)3 3) K2SO3 4) HClO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 53 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) FeCl2 2) HNO3 3) K3PO4 4) LiOH Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 54 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NaClO4 2) FeCl3 3) HClO4 4) KHCO3 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 55 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3 2) ZnCl2 3) K2SO4 4) HBr Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 56 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CuSO4 2) NaOH 3) K2SO3 4) Ca(NO3)2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 57 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) HF 2) NH3 3) (NH4)2SO4 4) Sr(OH)2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
| Задание 58 | |
| Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KNO2 2) LiOH 3) ZnSO4 4) Ba(NO3)2 Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая. |
Подготовка к ЕГЭ-2016 по химии (задание 30)
Проверяемый элемент содержания:
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Одним из важнейших свойств солей является гидролиз. Гидролизом называют взаимодействие ионов соли с водой, приводящее к образованию слабого электролита.
В зависимости от силы кислот и оснований образуемые ими соли делят на четыре типа:
1) соли, образованные катионом сильного основания и анионом сильной кислоты;
2) соли, образованные катионом сильного основания и анионом слабой кислоты;
3) соли, образованные катионом слабого основания и анионом сильной кислотой;
4) соли, образованные катионом слабого основания и анионом слабой кислотой.
|
Основания |
|
|
Сильные |
щелочи – LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2 |
|
Слабые |
как правило, нерастворимые основания – Mg(OH)2, AI(OH)3, Cr(OH)3, Fe(OH)2, Fe(OH)3, Zn(OH)2, Pb(OH)2, Cu(OH)2; гидрат аммиака NH3 · H2O (или NH4OH) |
|
Кислоты |
|
|
Сильные |
HNO3, HCI, HBr, HI, HCIO4, HMnO2, H2SO4 |
|
Слабые |
органические кислоты – HCOOH, CH3COOH, C6H5COOH; неорганические – HF, H2S, H2CO3, HNO2, HCN, H3BO3, HCIO, HCIO2, H2SiO3, Н3РО4 |
Типы солей
|
соли, образованные катионом сильного основания и анионом сильной кислоты |
Na2SO4, KNO3 |
|
соли, образованные катионом сильного основания и анионом слабой кислоты |
Na2CO3, CH3COOK |
|
соли, образованные катионом слабого основания и анионом сильной кислотой |
ZnCI2, Cu(NO3)2 |
|
соли, образованные катионом слабого основания и анионом слабой кислотой |
(NH4)2S, (CH3COO)2Cu |
Окраска индикаторов
|
Нейтральная среда |
Кислая среда |
Щелочная среда |
|
|
лакмус |
фиолетовый |
красный |
синий |
|
метиловый оранжевый |
оранжевый |
розовый |
желтый |
|
фенолфталеин |
бесцветный |
бесцветный |
малиновый |
|
рН |
рН = 7 |
рН < 7 |
рН > 7 |
Хотя гидролиз солей – разновидность реакции обмена, технология составления уравнений реакций этого процесса имеет свои особенности. Главное отличие – то, что в этом случае сначала составляют ионное уравнение реакции, а затем не его основе записывают молекулярное.
Алгоритм составления уравнения реакции гидролиза
ВНИМАНИЕ! Диссоциация молекул воды – не происходит. Уравнение диссоциации воды записывается только для того, чтобы правильно составить уравнение гидролиза!!!
- Анализируют состав соли:
NaOH (сильное основание)
Na2CO3
H2CO3 (слабая кислота)
- Выбирают ион, подвергающийся гидролизу:
Na2CO3 ↔ 2Na+ + CO32-
HOH ↔ H+ + OH—
2Na+ + CO32- + HOH ↔ 2Na+ + HCO3— + OH—
- Из полученного уравнения составляют молекулярное, используя те ионы, которые принимали участие в гидролизе:
Na2CO3 + HOH ↔ NaHCO3 + NaOH
среда раствора
соли – щелочная
- Данный алгоритм не относится к случаю так называемого полного гидролиза.
Типы солей и характер их гидролиза
- Соль образована катионом сильного основания и анионом сильной кислоты.
Соли этого типа гидролизу не подвергаются, так как при их взаимодействии с водой равновесие ионов H+ и ОН— не нарушается. В растворах таких солей среда остается нейтральной (рН = 7).
NaOH (сильное основание)
NaNO3
HNO3 (сильная кислота)
NaNO3 + HOH
- Соль, образованная катионом сильного основания и анионом слабой кислоты.
Гидролиз этого типа солей иначе называется гидролизом по аниону. Рассмотрим в качестве примера гидролиз K2SO3
KOH (сильное основание)
К2SO3
H2SO3 (слабая кислота)
K2SO3 ↔ 2K+ + SO32-
HOH ↔ H+ + OH—
2K+ + SO32- + HOH ↔ 2K+ + HSO3— + OH—
K2SO3 + HOH ↔ KHSO3 + KOH
среда раствора
соли – щелочная
Таким образом, каждый ион Н+ нейтрализует одну единицу отрицательного заряда иона кислотного остатка СО32-, а из молекулы воды НОН освобождаются гидроксид-ион ОН—. Эти ионы гидроксида ОН—, будучи в избытке, придают щелочную реакцию (рН>7).
Следовательно, растворы солей, образованные сильным основанием и слабой кислотой, имеют щелочную реакцию.
Данный случай гидролиза обратим.
- Соль, образованная катионом слабого основания и анионом сильной кислоты.
Гидролиз этого типа солей иначе называют гидролизом по катиону. Рассмотрим гидролиз хлорида меди (II) CuCI2
Cu(OH)2 (слабое основание)
СuSO4
H2SO4 (сильная кислота)
CuSO4 ↔ Cu2+ + SO42-
HOH ↔ H+ + OH—
Cu2+ + SO42- + HOH ↔ CuOH+ + SO42- + H+
2CuSO4 + 2HOH ↔ (CuOH)2SO4 + H2SO4
среда раствора
соли – кислая
В растворе наблюдается избыток ионов Н+. Следовательно, растворы солей, образованные слабым основанием и сильной кислотой, имеют кислую реакцию (рН<7).
Данный случай гидролиза также обратим.
- Соль, образованная катионом слабого основания и анионом слабой кислоты.
Гидролиз этого типа иначе называют гидролизом по катиону, и аниону. В соли слабого основания и слабой кислоты, например сульфиде алюминия AI2S3, катион ведет себя как кислота, а анион – как – основание:
AI2S3 + 6H2O = 2AI(OH)3 ↓ + 3H2S↑
Реакция идет полностью до конца и гидролиз необратим. Реакция и рН среды растворов данных солей зависит от относительной силы образующихся слабых кислот и оснований и может быть либо нейтральной, либо незначительно смещенной в ту или иную сторону, т.е. слабокислой или слабощелочной.
Смещение химического равновесия при гидролизе
На процесс гидролиза значительное влияние оказывают концентрация и температура. В соответствии с принципом Ле Шателье рассмотрим влияние этих факторов на положение гидролитического расщепления.
Разбавление раствора равноценно увеличению концентрации одного из реагирующих веществ (в данном случае воды). Следовательно, равновесие смещается вправо, т.е. гидролиз усиливается. Наоборот, гидролиз концентрированных растворов протекает значительно слабее.
Изменение температуры влияет на гидролиз вследствие резкой температурной зависимости степени диссоциации воды. С повышением температуры концентрация Н+ и ОН— ионов в растворе резко возрастает, вследствие чего увеличивается вероятность связывания их с образованием малодиссоциированной кислоты или основания. Поэтому с повышением температуры гидролиз протекает полнее.
Данный вывод подтверждается тем, что реакция нейтрализации экзотермична. Так как гидролиз является противоположным ей процессом, т.е. эндотермичен, то в соответствии с принципом Ле Шателье нагревание вызывает усиление гидролиза.
НЕОБРАТИМЫЙ ГИДРОЛИЗ НЕОРГАНИЧЕСКИХ И ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Необратимый гидролиз солей кислородсодержащих солей (катион слабого основания и анион слабой кислоты)
При сливании водных растворов карбоната натрия Na2CO3 и хлорида алюминия AICI3 выделяется газ и выпадает осадок. Что это за осадок и какой газ может выделяться в данной обменной реакции? Если мы посмотрим в таблицу растворимости, то в клетке, соответствующей карбонату алюминия, увидим прочерк. В данном случае это означает, что соль разлагается водой, т.е. протекает ее необратимый гидролиз.
В водном растворе и катион алюминия (соответствующий нерастворимому в воде гидроксиду), и карбонат-анион (соответствующий слабой кислоте) подвержены гидролизу. Гидролиз катиона AI3+ протекает с образованием катионов водорода, гидролиз аниона СО32- сопровождается выделением в раствор гидроксид-анионов. При сливании двух растворов за счет взаимного связывания ионов Н+ и ОН— происходит смещение равновесия обоих процессов вправо вплоть до необратимого протекания гидролиза:
AI3+ + H2O ↔ AIOH2+ + H+
CO32- + H2O ↔ HCO3— + OH—
3CO2↑
2AI3+ + 3CO32- + 6H2O ↔ 2AI(OH)3↓ + 3H2CO3
3H2O
Подобным образом полностью гидролизуются сульфиты алюминия и хрома (III), карбоната железа (III) и некоторые другие соли кислородсодержащих кислот. Их нельзя получить реакцией обмена между водными растворами двух солей, содержащих соответствующие ионы.
Необратимый гидролиз бинарных соединений металл – неметалл
Помимо некоторых солей кислородсодержащих кислот, необратимому гидролизу могут подвергаться соли кислот бескислородных. Например, сульфиды алюминия, хрома (III), железа (III) при попадании в воду выделяют сероводород и образуют нерастворимое в воде основание:
Fe2S3 + 6H2O = 2Fe(OH)3↓ + 3H2S↑
Аналогично необратимо гидролизуются карбиды, нитриды, фосфиды активных металлов:
CaC2 + 2H2O = C2H2↑ + Ca(OH)2
Карбид кальция ацетилен
AI4C3 + 12H2O = 3CH4↑ + 4AI(OH)3↓
Карбид алюминия метан
Li3N + 3H2O = NH3 + 3LiOH
Нитрид лития Аммиак
Mg3P2 + 6H2O = 2PH3 + 3Mg(OH)2↓
Фосфид магния Фосфин
Необратимый гидролиз двухэлементных (бинарных) соединений неметаллов
Многие бинарные соединения неметаллов «не выдерживают» испытания водой и необратимо гидролизуются с образованием, как правило, двух кислот: кислородсодержащей (менее электроотрицательный элемент в бинарном соединении) и бескислородной (более электроотрицательный элемент).
SiCI4 + 3H2O = H2SiO3 + 4HCI
P2S5 + 8H2O = 2H3PO4 + 5H2S
Гидролиз органических соединений
О
//
СН3 – С + Н2О = СН3 – СООН + HCI
Уксусная кислота
СI
Ацетилхлорид
В живых организмах одним из путей метаболизма жиров является их гидролиз. В кишечнике под влиянием фермента липазы жиры распадаются на глицерин и органические кислоты, которые всасываются стенками кишечника, и в организме синтезируются новые жиры, свойственные данному организму:
СН2 – О – СО – С17Н35 СН2 – ОН
│ │
СН – О – СО – С17Н35 + 3Н2О ↔ СН – ОН + 3С17Н35СООН
│ │
СН2 – О – СО – С17Н35 СН2 – ОН
Тристеарат глицерина Глицерин Стеариновая кислота
Большое значение имеет также гидролиз углеводов. Углеводы, содержащие два и более остатка моносахаридов (вплоть до полисахаридов), подвергаются гидролизу. Конечными продуктами такого процесса являются составляющие молекулу моносахариды.
Гидролиз дисахаридов, например сахарозы, можно представить следующей схемой:
С12Н22О11 + Н2О = С6Н12О6 + С6Н12О6
сахароза глюкоза фруктоза
Полисахариды гидролизуются ступенчато:
+Н2О +Н2О +Н2О
(С6Н10О5)n (C6H10O5)x C12H22O11 C6H12O6
крахмал декстрины (х
Гидролиз углеводов катализируется кислотами, а в живых организмах – ферментами. В промышленности гидролизом крахмала получают глюкозу и патоку (смесь декстринов, мальтозы и глюкозы).
Гораздо труднее гидролизуется другой важнейший полисахарид – целлюлоза. Гидролиз целлюлозы в промышленности проводят при длительном кипячении непищевого растительного сырья в присутствии кислоты: отходов лесозаготовки и деревообработки. Процесс также идет ступенчато:
(С6Н10О5)n + nН2О = n C6H12O6
Целлюлоза глюкоза
Также гидролизу подвергаются белки.
СОЛИ ФОСФОРНОЙ КИСЛОТЫ
Растворимые средние соли фосфорной кислоты подвергаются гидролизу по аниону кислоты и их растворы имеют сильно щелочную реакцию:
Na3PO4 + HOH → Na2HPO4 + NaOH
HOH + PO43- → HPO42- + OH—
Кислые соли фосфорной кислоты (особенно дигидрофосфаты) гидролизуются в значительно меньшей степени, кроме того, образующиеся при этом продукты гидролиза: H2PO4–, H3PO4 – могут частично диссоциировать с образованием ионов Н+. Поэтому в растворах гидрофосфатов среда является слабощелочной, а в растворах дигидрофосфатов даже слабокислой, т.к. процесс диссоциации H2PO4–-ионов превалирует над процессом их гидролиза.
Тренировочные задания:
|
1. |
Установите соответствие между названием соли и её отношением к гидролизу |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ К ГИДРОЛИЗУ |
|||||||
|
А) |
хлорид аммония |
1) |
гидролизуется по катиону |
|||||
|
Б) |
сульфат калия |
2) |
гидролизуется по аниону |
|||||
|
В) |
карбонат натрия |
3) |
гидролизу не подвергается |
|||||
|
Г) |
сульфид алюминия |
4) |
гидролизуется по катиону и аниону |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
2. |
Установите соответствие между названием соли и способностью ее к гидролизу |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ К ГИДРОЛИЗУ |
|||||||
|
А) |
хлорид аммония |
1) |
гидролизу не подвергается |
|||||
|
Б) |
сульфат калия |
2) |
гидролизуется по катиону |
|||||
|
В) |
карбонат натрия |
3) |
гидролизуется по аниону |
|||||
|
Г) |
сульфид алюминия |
4) |
гидролизуется по катиону и аниону |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
3. |
Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое. |
|||||||
|
ПЕРВАЯ СОЛЬ |
ВТОРАЯ СОЛЬ |
|||||||
|
А) |
перманганат натрия |
1) |
хлорид калия |
|||||
|
Б) |
хлорид меди (II) |
2) |
фосфид алюминия |
|||||
|
В) |
сульфат аммония |
3) |
фосфат натрия |
|||||
|
Г) |
перхлорат калия |
4) |
нитрат цинка |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
4. |
Установите соответствие между названием соли и способностью ее к гидролизу |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ К ГИДРОЛИЗУ |
|||||||
|
А) |
пропионат цезия |
1) |
гидролизу не подвергается |
|||||
|
Б) |
нитрат диметиламмония |
2) |
гидролизуется по катиону |
|||||
|
В) |
карбонат калия |
3) |
гидролизуется по аниону |
|||||
|
Г) |
сульфат аммония |
4) |
гидролизуется по катиону и аниону |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
5. |
Установите соответствие между названием соли и способностью ее к гидролизу |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ К ГИДРОЛИЗУ |
|||||||
|
А) |
фторид цезия |
1) |
гидролизу не подвергается |
|||||
|
Б) |
нитрат калия |
2) |
гидролизуется по катиону |
|||||
|
В) |
нитрит натрия |
3) |
гидролизуется по аниону |
|||||
|
Г) |
сульфид аммония |
4) |
гидролизуется по катиону и аниону |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
6. |
Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое. |
|||||||
|
ПЕРВАЯ СОЛЬ |
ВТОРАЯ СОЛЬ |
|||||||
|
А) |
сульфит натрия |
1) |
сульфат рубидия |
|||||
|
Б) |
фторид алюминия |
2) |
нитрат железа (II) |
|||||
|
В) |
сульфат цинка |
3) |
ортофосфат калия |
|||||
|
Г) |
нитрат кальция |
4) |
ацетат алюминия |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
7. |
Установите соответствие между названием соли и средой ее водного раствора |
|||||||
|
НАЗВАНИЕ СОЛИ |
СРЕДА РАСТВОРА |
|||||||
|
А) |
сульфид калия |
1) |
нейтральная |
|||||
|
Б) |
гидрофосфат натрия |
2) |
кислая |
|||||
|
В) |
дигидрофосфат цезия |
3) |
щелочная |
|||||
|
Г) |
сульфат цинка |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
8. |
Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое. |
|||||||
|
ПЕРВАЯ СОЛЬ |
ВТОРАЯ СОЛЬ |
|||||||
|
А) |
сульфид калия |
1) |
сульфат калия |
|||||
|
Б) |
сульфид алюминия |
2) |
хлорид цинка |
|||||
|
В) |
сульфат железа (II) |
3) |
ортофосфат натрия |
|||||
|
Г) |
нитрат бария |
4) |
ацетат метиламмония |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
9. |
Установите соответствие между названием соли и средой ее водного раствора |
|||||||
|
НАЗВАНИЕ СОЛИ |
СРЕДА РАСТВОРА |
|||||||
|
А) |
нитрит калия |
1) |
нейтральная |
|||||
|
Б) |
хлорацетат натрия |
2) |
кислая |
|||||
|
В) |
гидрокарбонат рубидия |
3) |
щелочная |
|||||
|
Г) |
сульфат алюминия |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
10. |
Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое. |
|||||||
|
ПЕРВАЯ СОЛЬ |
ВТОРАЯ СОЛЬ |
|||||||
|
А) |
сульфат калия |
1) |
сульфид калия |
|||||
|
Б) |
хлорид железа (II) |
2) |
сульфид алюминия |
|||||
|
В) |
ортофосфат натрия |
3) |
сульфат хрома (II) |
|||||
|
Г) |
ацетат метиламмония |
4) |
нитрат бария |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
11. |
Установите соответствие между названием соли и средой ее водного раствора |
|||||||
|
НАЗВАНИЕ СОЛИ |
СРЕДА РАСТВОРА |
|||||||
|
А) |
сульфит натрия |
1) |
нейтральная |
|||||
|
Б) |
ацетат калия |
2) |
кислая |
|||||
|
В) |
фторид рубидия |
3) |
щелочная |
|||||
|
Г) |
хлорид алюминия |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
12. |
Установите соответствие между названием соли и типом гидролиза этой соли |
|||||||
|
НАЗВАНИЕ СОЛИ |
ТИП ГИДРОЛИЗА |
|||||||
|
А) |
ортофосфат натрия |
1) |
по катиону |
|||||
|
Б) |
гидрокарбонат кальция |
2) |
по аниону |
|||||
|
В) |
карбонат аммония |
3) |
по катиону и аниону |
|||||
|
Г) |
нитрат цинка |
4) |
гидролиз отсутствует |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
13. |
Установите соответствие между названием вещества и средой его водного раствора. |
|||||||
|
ВЕЩЕСТВО |
СРЕДА ВОДНОГО РАСТВОРА |
|||||||
|
А) |
иодид бария |
1) |
кислотная |
|||||
|
Б) |
иодоводород |
2) |
нейтральная |
|||||
|
В) |
гидроксид кальция |
3) |
щелочная |
|||||
|
Г) |
бромид железа (II) |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
14. |
Установите соответствие между названием соли и отношением ее к гидролизу |
|||||||
|
НАЗВАНИЕ СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
нитрат натрия |
1) |
гидролиз по катиону |
|||||
|
Б) |
карбонат калия |
2) |
гидролиза по аниону |
|||||
|
В) |
сульфид алюминия |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
хлорид аммония |
4) |
гидролизу не подвергается |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
15. |
Установите соответствие между названием вещества и средой его водного раствора. |
|||||||
|
ВЕЩЕСТВО |
СРЕДА ВОДНОГО РАСТВОРА |
|||||||
|
А) |
сульфит калия |
1) |
нейтральная |
|||||
|
Б) |
гидросульфид калия |
2) |
кислотная |
|||||
|
В) |
нитрат аммония |
3) |
щелочная |
|||||
|
Г) |
сероводород |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
16. |
Установите соответствие между формулой соли и средой ее водного раствора. |
|||||||
|
ФОРМУЛА СОЛИ |
СРЕДА РАСТВОРА |
|||||||
|
А) |
Na2S |
1) |
кислотная |
|||||
|
Б) |
Na2SO4 |
2) |
нейтральная |
|||||
|
В) |
BeSO4 |
3) |
щелочная |
|||||
|
Г) |
NaHSO4 |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
17. |
Установите соответствие между названием соли и средой в водном растворе этой соли. |
|||||||
|
НАЗВАНИЕ СОЛИ |
СРЕДА ВОДНОГО РАСТВОРА СОЛИ |
|||||||
|
А) |
сульфат цинка |
1) |
кислотная |
|||||
|
Б) |
карбонат натрия |
2) |
нейтральная |
|||||
|
В) |
сульфат аммония |
3) |
щелочная |
|||||
|
Г) |
гидрокарбонат натрия |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
18. |
Установите соответствие между названием вещества и средой его водного раствора. |
|||||||
|
НАЗВАНИЕ ВЕЩЕСТВА |
СРЕДА ВОДНОГО РАСТВОРА |
|||||||
|
А) |
сульфид бария |
1) |
кислотная |
|||||
|
Б) |
хлорид стронция |
2) |
нейтральная |
|||||
|
В) |
хлороводород |
3) |
щелочная |
|||||
|
Г) |
гидроксид натрия |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
19. |
Установите соответствие между названием соли и ее способностью к гидролизу |
|||||||
|
НАЗВАНИЕ СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
ацетат аммония |
1) |
гидролиз по катиону |
|||||
|
Б) |
бромид аммония |
2) |
гидролиза по аниону |
|||||
|
В) |
сульфат натрия |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
хлорид железа (III) |
4) |
гидролизу не подвергается |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
20. |
Установите соответствие между формулой соли и ее способностью к гидролизу. |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
(NH4)(CH3COO) |
1) |
гидролиз по катиону |
|||||
|
Б) |
NH4Br |
2) |
гидролиза по аниону |
|||||
|
В) |
Na2SO4 |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
FeSO4 |
4) |
гидролизу не подвергается |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
21. |
Установите соответствие между формулой соли и средой ее водного раствора. |
|||||||
|
ФОРМУЛА СОЛИ |
СРЕДА ВОДНОГО РАСТВОРА |
|||||||
|
А) |
Na2SO4 |
1) |
нейтральная |
|||||
|
Б) |
CuSO4 |
2) |
кислотная |
|||||
|
В) |
NaCIO4 |
3) |
щелочная |
|||||
|
Г) |
Ba(CIO)2 |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
22. |
Установите соответствие между названием соли и ее отношением к гидролизу |
|||||||
|
НАЗВАНИЕ СОЛИ |
ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|||||||
|
А) |
сульфид алюминия |
1) |
гидролиз по катиону |
|||||
|
Б) |
карбонат натрия |
2) |
гидролиз не происходит |
|||||
|
В) |
сульфат аммония |
3) |
гидролиз по аниону |
|||||
|
Г) |
гидрокарбонат натрия |
4) |
необратимый гидролиз |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
23. |
Установите соответствие между названием соли и типом гидролиза этой соли |
|||||||
|
НАЗВАНИЕ СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
ортофосфат натрия |
1) |
по катиону |
|||||
|
Б) |
сульфат алюминия |
2) |
по аниону |
|||||
|
В) |
нитрит калия |
3) |
по катиону и аниону |
|||||
|
Г) |
сульфат аммония |
4) |
отсутствует |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
24. |
Установите соответствие между названием соли и рН среды при ее гидролизе. |
|||||||
|
НАЗВАНИЕ СОЛИ |
рН СРЕДЫ ПРИ ГИДРОЛИЗЕ |
|||||||
|
А) |
сульфит калия |
1) |
рН > 7 |
|||||
|
Б) |
хлорид меди |
2) |
рН < 7 |
|||||
|
В) |
сульфат натрия |
3) |
рН = 7 |
|||||
|
Г) |
нитрит лития |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
25. |
Установите соответствие между названием соли и типом гидролиза ее в водном растворе. |
|||||||
|
НАЗВАНИЕ СОЛИ |
ТИП ГИДРОЛИЗА |
|||||||
|
А) |
карбонат натрия |
1) |
по катиону |
|||||
|
Б) |
нитрат цинка |
2) |
по аниону |
|||||
|
В) |
фторид натрия |
3) |
по катиону и аниону |
|||||
|
Г) |
сульфид калия |
4) |
гидролиз не происходит |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
26. |
Установите соответствие между названием соли и отношением ее к гидролизу |
|||||||
|
НАЗВАНИЕ СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
ацетат натрия |
1) |
гидролиз по катиону |
|||||
|
Б) |
хлорид калия |
2) |
гидролиза по аниону |
|||||
|
В) |
нитрит аммония |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
нитрат железа (III) |
4) |
гидролизу не подвергается |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
27. |
Установите соответствие между формулой соли и ее способностью к гидролизу |
|||||||
|
ФОРМУЛА СОЛИ |
СПОСОБНОСТЬ СОЛИ К ГИДРОЛИЗУ |
|||||||
|
А) |
NaCH3COO |
1) |
гидролиз по катиону |
|||||
|
Б) |
KCI |
2) |
гидролиза по аниону |
|||||
|
В) |
KNO2 |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
Fe(NO3)3 |
4) |
гидролизу не подвергается |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
28. |
Установите соответствие между формулой соли и средой ее водного раствора |
|||||||
|
ФОРМУЛА СОЛИ |
СРЕДА ВОДНОГО РАСТВОРА |
|||||||
|
А) |
Na2CO3 |
1) |
нейтральная |
|||||
|
Б) |
NaHCO3 |
2) |
кислотная |
|||||
|
В) |
Fe(CIO4)2 |
3) |
щелочная |
|||||
|
Г) |
NH4CIO4 |
|||||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
29. |
Установите соответствие между названием соли и типом гидролиза этой соли |
|||||||
|
НАЗВАНИЕ СОЛИ |
ТИП ГИДРОЛИЗА |
|||||||
|
А) |
дигидрофосфат натрия |
1) |
гидролиз по катиону |
|||||
|
Б) |
гидрофосфат натрия |
2) |
гидролиза по аниону |
|||||
|
В) |
фторид натрия |
3) |
гидролиз по катиону и аниону |
|||||
|
Г) |
ацетат натрия |
4) |
гидролиз не происходит |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
|
30. |
Установите соответствие между названием соли и типом ее гидролиза вводном растворе. |
|||||||
|
НАЗВАНИЕ СОЛИ |
ТИП ГИДРОЛИЗА |
|||||||
|
А) |
карбонат калия |
1) |
по катиону |
|||||
|
Б) |
нитрат железа (III) |
2) |
по аниону |
|||||
|
В) |
гидрокарбонат кальция |
3) |
по катиону и аниону |
|||||
|
Г) |
бромид железа (II) |
4) |
гидролиз отсутствует |
|||||
|
А |
Б |
В |
Г |
|||||
|
Ответ: |
ОТВЕТЫ:
1 – 1324
2 – 3334
3 – 1441
4 – 3232
5 – 3134
6 – 3421
7 – 3322
8 – 3421
9 – 3332
10 – 4312
11 – 3332
12 – 2231
13 – 2131
14 – 4231
15 – 3322
16 – 3211
17 – 1313
18 – 3213
19 – 3142
20 – 3141
21 – 1213
22 – 4313
23 – 2121
24 – 1231
25 – 2122
26 – 2431
27 – 2421
28 – 3322
29 – 2222
30 – 2121
- ЕГЭ по химии
Вопрос №21 ЕГЭ. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная.
Подборка заданий на pH и гидролиз в новом формате ЕГЭ 2022 по химии.
→ скачать задания
→ Проверить ответы
Источник: vk.com/chem4you
Примеры заданий:
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) Гидросульфат натрия
2) Гидросульфид калия
3) Нитрат бария
4) Гидроксид лития
Запишите номера веществ в порядке убывания значения pH их водных растворов.
Вещества, приведенные в перечне, растворили в воде и получили растворы с одинаковой молярной (моль/л) концентрацией веществ. Определите характер среды полученных растворов.
1) SiCl4
2) Na3PO4 · 12H2O
3) KClO3
4) Ba3P2
Запишите номера веществ в порядке возрастания значения pH растворов, полученных при внесении данных веществ в воду.
Смотрите также:
Задания – тренажёры по химии 11 класс
по теме «Гидролиз»
1. Установите соответствие между названием соли и типом гидролиза
1) хлорид цинка а) гидролизуется по катиону
2) сульфид калия б) гидролизуется по аниону
3) нитрат натрия в) гидролизуется и по катиону и по аниону
4) нитрат меди г) не гидролизуется
2. Установите соответствие между названием соли и средой её водного раствора
1) сульфид алюминия а) по катиону
2) сульфид натрия б) по аниону
3) нитрат магния в) по катиону и аниону
4) сульфит калия
3. Установите соответствие между формулой соли и средой её водного раствора
1) K2SO4 а) нейтральная
2) CrCl3 б) кислая
3) Li2CO3 в) щелочная
4) NH4Br
4. Установите соответствие между названием соли и средой её водного раствора
1) нитрат бария а) кислая
2) хлорид железа (III) б) нейтральная
3) сульфат аммония в) щелочная
4) ацетат калия
5. Установите соответствие между формулой соли и молекулярно-ионным уравнением гидролиза этой соли
1) CuSO4 а) CH3COO– + H2O = CH3COOH + OH–
2) K2CO3 б) NH4+ + H2O = NH3H2O + H+
3) CH3COONa в) Сu2+ + H2O = Cu(OH)+ + H+
4) (NH4)2SO4 г) СO32– + H2O = HCO3– + OH–
д) Сu2+ + 2H2O = Cu(OH)2 + 2H+
6. Установите соответствие между названием соли и средой её водного раствора
1) ацетат калия а) кислая
2) сульфит натрия б) нейтральная
3) нитрат лития в) щелочная
4) хлорид цинка
7. Установите соответствие между названием соли и средой её водного раствора
1) формиат натрия а) кислая
2) хлорид бария б) нейтральная
3) нитрит калия в) щелочная
4) нитрат ртути(II)
8. Установите соответствие между названием соли и типом гидролиза
1) пропионат аммония а) гидролиз по катиону
2) сульфид цезия б) гидролиз по аниону
3) сульфид алюминия в) гидролиз по катиону и аниону
4) карбонат натрия г) гидролизу не подвергается
9. Установите соответствие между названием соли и типом гидролиза
1) карбонат натрия а) гидролиз по катиону
2) хлорид аммония б) гидролиз по аниону
3) сульфат калия в) гидролиз по катиону и аниону
4) сульфид алюминия г) гидролизу не подвергается
10. Установите соответствие между формулой соли и молекулярно-ионным уравнением гидролиза этой соли
1) Na2SiO3 a) Na+ + H2O = NaOH + H+
2) Al(NO3)3 б) Al3+ + H2O = AlOH2+ + H+
3) CH3COONa в) NH4+ + H2O = NH3 + H3O+
4) NH4NO3 г) СН3СОО — + H2O = СН 3СОOH + H+
д) СН3СОО — + H2O = СН 3СОOH + OH —
е) СН3СОО Na + H2O = СН 3СОOH + Na + OH —
ж) NO3— + H2O = HNO3 + OH —
з) SiO32- + H2O = HSiO3 — + OH —
11. Установите соответствие между названием соли и типом гидролиза
1) хлорид аммония а) гидролизуется по аниону
2) сульфат калия б) гидролизуется по катиону
3) карбонат натрия в) гидролиз не происходит
4) сульфид алюминия г) необратимый гидролиз
12. Установите соответствие между формулой соли и её способностью к гидролизу
1) Сr2(S04)з а) гидролиз по катиону
2) Na 2SO4 б) гидролиз по аниону
3) ВаСl2 в) гидролиз по катиону и аниону
4) AI 2S3 г) гидролизу не подвергается
13 Установите соответствие между названием соли и отношением ее к гидролизу
1) хлорид цинка а) гидролизуется по катиону
2) сульфид калия б) гидролизуется по аниону
3) нитрат натрия в) гидролизуется по катиону и аниону
4) нитрат меди г) не гидролизуется
14. Установите соответствие между формулой соли и типом её гидролиза
1) BeSO4 а) по катиону
2) KNO2 б) по аниону
3) CuCl2 в) по катиону и по аниону
4) Pb (NO3)2 г) не гидролизуется
15. Установите соответствие между названием соли и её способностью к гидролизу
1) хлорид аммония а) гидролиз по катиону
2) сульфат калия б) гидролиз по аниону
3) карбонат натрия в) гидролиз не происходит
4) карбонат железа(III) г) необратимый гидролиз
-
Установите соответствие между названием соли и кислотностью среды в растворе этой соли
1) нитрит калия а) нейтральная
2) фенолят натрия б) кислая
3) хлорид аммония в) щелочная
4) сульфат калия
-
Установите соответствие между формулой соли и её способностью к гидролизу
1) FeCl3 а) по катиону
2) BaS б) по аниону
3) KF в) по катиону и по аниону
4) ZnSO4 г) не гидролизуется
18. Установите соответствие между формулой соли и окраской индикатора лакмуса в её водном растворе.
1) Cu (NO3)2 а) красная
2) Li2S б) синяя
3) Na2SO3 в) фиолетовая
4) CaCl2 г) не окрашен
19. Установите соответствие между названием соли и её способностью к гидролизу
1) нитрат железа(II) а) гидролиз по катиону
2) сульфат меди б) гидролиз по аниону
3) сульфид бария в) гидролиз не происходит
4) нитрат кальция г) гидролиз по катиону и аниону
20. Установите соответствие между формулой соли и окраской индикаторов в её водном растворе.
1) KF а) лакмус красный, фенолфталеин красный
2) Al2(S04)з б) лакмус красный, фенолфталеин бесцветный
3) KCl в) лакмус синий, фенолфталеин красный
4) Na 3PO4 г) лакмус синий, фенолфталеин бесцветный
д) лакмус фиолетовый, фенолфталеин красный
21. Установите соответствие между названиями веществ и продуктами их гидролиза
1) трипальмитин а) C15H31COOH и C3H5(OH)3
2) нитрид кальция б) ZnOHCl и HCl
3) хлорид цинка в)NH3 и Ca(OH)2
4) триацетат целлюлозы г) (C6H10O5)n и CH3COOH
д) Ca(NO3)2 и NH3
е) Zn(OH)2 и HCl
22. Установите соответствие между названием соли и цветом индикаторов в растворе этой соли.
1) нитрат бария а) фенолфталеин красный, лакмус синий
2) хлорид железа(III) б) фенолфталеин бесцветный, лакмус красный
3) сульфат аммония в) фенолфталеин бесцветный, лакмус фиолетовый
4) ацетат калия г) фенолфталеин красный, лакмус красный
23. Установите соответствие между названием соли и средой её водного раствора
1) хлорид хрома(III) а) нейтральная
2) сульфат хрома (II) б) кислая
3) сульфид натрия в) щелочная
4) сульфат цезия
24. Установите соответствие между названием соли и её способностью к гидролизу
1) сульфат рубидия а) гидролизу не подвергается
2) сульфид аммония б) гидролизуется по катиону
3) фосфат калия в) гидролизуется по аниону
4) сульфид лития г) гидролизуется по катиону и по аниону
25. Установите соответствие между названием соли и её способностью к гидролизу
1) сульфид натрия а) гидролизу не подвергается
2) нитрат бария б) гидролизуется по катиону
3) сульфат калия в) гидролизуется по аниону
4) карбонат аммония г) гидролизуется по катиону и по аниону
26. Установите соответствие между названием соли и её способностью к гидролизу
1) стеарат аммония а) гидролизу не подвергается
2) пальмитат калия б) гидролизуется по катиону
3) перхлорат натрия в) гидролизуется по аниону
4) сульфат цезия г) гидролизуется по катиону и по аниону
27. Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое
1) сульфат натрия а) сульфид калия
2) хлорид алюминия б) сульфид аммония
3) ортофосфат цезия в) сульфат железа (II)
4) ацетат аммония г) нитрат бария
28. Установите соответствие между названиями веществ и рН их водного раствора
1) гидроксид лития, сульфид калия,
силикат натрия а) рН больше 7
2) хлорид бария, хромат калия, б) рН меньше 7
перманганат натрия в) рН равно 7
3) формиат натрия, нитрит калия, г) нет однозначного ответа
гипохлорит кальция
4) хлорид кадмия(II), сульфат хрома (III),
нитрат аммония
29. Установите соответствие между формулами веществ и рН среды, характерной для их водных растворов
1) NH4Cl, FeBr3, CdSO4 а) рН больше 7
2) Na(HCOO), Cs2S, LiNO2 б) рН меньше 7
3) NaMnO4, KCLO4, K2Cr2O7 в) рН равно 7
4) (NH4)2Cr2O7, BeI2, ZnCl2 г) нет однозначного ответа
30. Установите соответствие между двумя солями, отношение которых к гидролизу одинаковое
1) Fe2(CO3)3 а) K2S
2) NaCl б) (NH4)2SiO3
3) Cs3PO4 в) FeSO4
4) NH4NO3 д) Ba(NO3)2
Таблица правильных ответов:
|
1 |
абга |
11 |
бваг |
21 |
авег |
|
2 |
вбаб |
12 |
аггв |
22 |
вбба |
|
3 |
абвб |
13 |
абга |
23 |
ббва |
|
4 |
баав |
14 |
абаа |
24 |
агвв |
|
5 |
вгаб |
15 |
авбг |
25 |
вааг |
|
6 |
ввба |
16 |
ввба |
26 |
гваа |
|
7 |
вбва |
17 |
абба |
27 |
гваб |
|
8 |
вбвб |
18 |
аббв |
28 |
аваб |
|
9 |
багв |
19 |
аабв |
29 |
бабв |
|
10 |
збдв |
20 |
вббв |
30 |
бдав |
Тематический тренировочный тест на гидролиз солей.
Задание №1
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. KCl
- 2. Fe(NO3)3
- 3. BaBr2
- 4. ZnCl2
- 5. NaI
Решение
Ответ: 24
Задание №2
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. RbHS
- 2. Ca(NO3)2
- 3. FeSO4
- 4. BeSO4
- 5. SrCl2
Решение
Ответ: 134
Задание №3
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Na2CO3
- 2. LiCl
- 3. KHCO3
- 4. FeI2
- 5. Al2(SO4)3
Решение
Ответ: 1345
Задание №4
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. HgCl2
- 2. CsI
- 3. NaF
- 4. CuSO4
- 5. Mg(NO3)2
Решение
Ответ: 1345
Задание №5
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Zn(CH3COO)2
- 2. NH4Cl
- 3. BaSO4
- 4. AlBr3
- 5. Cr(NO3)3
Решение
Ответ: 1245
Задание №6
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. NaHSO4
- 2. Fe2(SO4)3
- 3. CrCl3
- 4. Mn(NO3)2
- 5. RbNO3
Решение
Ответ: 234
Задание №7
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Ba(NO3)2
- 2. BeBr2
- 3. KClO3
- 4. CuCl2
- 5. ZnSO4
Решение
Ответ: 245
Задание №8
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Na2HPO4
- 2. CaSO4
- 3. CuCl2
- 4. Cs2SO4
- 5. KI
Решение
Ответ: 13
Задание №9
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. KMnO4
- 2. K2SO4
- 3. LiClO3
- 4. NaClO4
- 5. BeCl2
Решение
Ответ: 5
Задание №10
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. KF
- 2. KClO
- 3. NaClO2
- 4. RbClO3
- 5. Zn(NO3)2
Решение
Ответ: 1235
[adsp-pro-3]
Задание №11
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. MnCl2
- 2. Mg(CH3COO)2
- 3. NH4NO3
- 4. KNO3
- 5. Cr2(SO4)3
Решение
Ответ: 1235
Задание №12
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. CuBr2
- 2. Na2S
- 3. KF
- 4. KI
- 5. Sr(NO3)2
Решение
Ответ: 123
Задание №13
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. FeSO4
- 2. CrSO4
- 3. MnSO4
- 4. K2SO4
- 5. NaHCO3
Решение
Ответ: 1235
Задание №14
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. KCl
- 2. NaClO3
- 3. CsCl
- 4. Sr(NO3)2
- 5. BeSO4
Решение
Ответ: 5
Задание №15
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. K2HPO4
- 2. ZnI2
- 3. MgSO4
- 4. Cu(NO3)2
- 5. KF
Решение
Ответ: 12345
Задание №16
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Pb(NO3)2
- 2. BaCO3
- 3. KNO2
- 4. MnSO4
- 5. Hg(NO3)2
Решение
Ответ: 1345
Задание №17
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Na2SiO3
- 2. NaHCO3
- 3. Na2SO4
- 4. Na3PO4
- 5. Na2SO3
Решение
Ответ: 1245
Задание №18
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. KClO3
- 2. LiClO4
- 3. NH4ClO4
- 4. BaCl2
- 5. NaClO
Решение
Ответ: 35
Задание №19
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. Cr2(SO4)3
- 2. Al(NO3)3
- 3. MnCl2
- 4. SrCl2
- 5. Rb2S
Решение
Ответ: 1235
Задание №20
Выберите соли, способные подвергаться гидролизу в водном растворе. Число верных ответов может быть любым
- 1. NaF
- 2. CaCO3
- 3. KClO2
- 4. FeCl3
- 5. Cr2(SO4)3
Решение
Ответ: 1345
[adsp-pro-3]
Задание №21
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) NaF Б) Na3PO4 В) KCl |
1) кислая 2) нейтральная 3) щелочная |
Решение
Ответ: 332
Задание №22
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) MgBr2 Б) BeCl2 В) K3PO4 |
1) щелочная 2) кислая 3) нейтральная |
Решение
Ответ: 221
Задание №23
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) MnCl2 Б) KClO3 В) Na3PO4 |
1) щелочная 2) кислая 3) нейтральная |
Решение
Ответ: 231
Задание №24
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) NH4NO3 Б) Ca(CH3COO)2 В) Cr2(SO4)3 |
1) нейтральная 2) кислая 3) щелочная |
Решение
Ответ: 232
Задание №25
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) CsI Б) Cr(NO3)3 В) NH4Cl |
1) кислая 2) нейтральная 3) щелочная |
Решение
Ответ: 211
Задание №26
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) Fe(NO3)3 Б) Rb2S В) ZnCl2 |
1) щелочная 2) кислая 3) нейтральная |
Решение
Ответ: 212
Задание №27
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) KClO Б) KNO3 В) KF |
1) нейтральная 2) щелочная 3) кислая |
Решение
Ответ: 212
Задание №28
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) K3PO4 Б) KNO2 В) Cu(NO3)2 |
1) кислая 2) щелочная 3) нейтральная |
Решение
Ответ: 221
Задание №29
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) MnCl2 Б) Cr2(SO4)3 В) NaI |
1) кислая 2) нейтральная 3) щелочная |
Решение
Ответ: 112
Задание №30
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) BeBr2 Б) ZnSO4 В) CuCl2 |
1) щелочная 2) нейтральная 3) кислая |
Решение
Ответ: 333
[adsp-pro-3]
Задание №31
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) Na2SO4 Б) K2CO3 В) CrCl3 |
1) щелочная 2) кислая 3) нейтральная |
Решение
Ответ: 312
Задание №32
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) BeBr2 Б) SnCl2 В) Rb2S |
1) кислая 2) нейтральная 3) щелочная |
Решение
Ответ: 113
Задание №33
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) Ca(CH3COO)2 Б) Cu(NO3)2 В) NH4Br |
1) кислая 2) щелочная 3) нейтральная |
Решение
Ответ: 211
Задание №34
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) FeSO4 Б) Na2CO3 В) FeBr2 |
1) нейтральная 2) щелочная 3) кислая |
Решение
Ответ: 323
Задание №35
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) KCl Б) NH4I В) BaBr2 |
1) щелочная 2) нейтральная 3) кислая |
Решение
Ответ: 232
Задание №36
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) FeSO4 Б) K2SO4 В) CsCl |
1) щелочная 2) кислая 3) нейтральная |
Решение
Ответ: 233
Задание №37
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) BeI2 Б) Cs2CO3 В) CuCl2 |
1) кислая 2) щелочная 3) нейтральная |
Решение
Ответ: 121
Задание №38
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) CuSO4 Б) LiClO4 В) BaCl2 |
1) кислая 2) нейтральная 3) щелочная |
Решение
Ответ: 122
Задание №39
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) Ba(NO3)2 Б) CaCl2 В) K3PO4 |
1) нейтральная 2) кислая 3) щелочная |
Решение
Ответ: 113
Задание №40
Установите соответствие между формулой соли и средой ее водного раствора
| ФОРМУЛА СОЛИ | СРЕДА РАСТВОРА |
|
А) Na2SiO3 Б) K2SO4 В) Rb2SO3 |
1) кислая 2) щелочная 3) нейтральная |
Решение
Ответ: 232
[adsp-pro-3]
Задание №41
Установите соответствие между солью и ее способностью к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) NaF Б) Na3PO4 В) KCl |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется и по катиону, и по аниону 4) гидролизу не подвергается |
Решение
Ответ: 224
Задание №42
Установите соответствие между солью и типом ее гидролиза
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) хлорид калия Б) сульфид аммония В) ацетат свинца |
1) гидролизу не подвергается 2) гидролизуется по катиону 3) гидролизуется по аниону 4) гидролизуется и по катиону, и по аниону |
Решение
Ответ: 144
Задание №43
Установите соответствие между солью и типом ее гидролиза
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) MnCl2 Б) KClO3 В) Na3PO4 |
1) гидролизуется и по катиону, и по аниону 2) гидролизу не подвергается 3) гидролизуется по катиону 4) гидролизуется по аниону |
Решение
Ответ: 324
Задание №44
Установите соответствие между солью и типом ее гидролиза
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) фторид калия Б) сульфат меди В) нитрат алюминия |
1) гидролизуется по аниону 2) гидролизуется и по катиону, и по аниону 3) гидролизу не подвергается 4) гидролизуется по катиону |
Решение
Ответ: 144
Задание №45
Установите соответствие между солью и типом ее гидролиза
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) CsI Б) Cr(NO3)3 В) NH4Cl |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) по катиону и аниону 4) гидролизу не подвергается |
Решение
Ответ: 411
Задание №46
Установите соответствие между солью и типом ее гидролиза
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) бромид лития Б) карбонат цезия В) нитрат стронция |
1) гидролизу не подвергается 2) гидролизуется по катиону 3) гидролизуется по аниону 4) гидролизуется и по катиону, и по аниону |
Решение
Ответ: 131
Задание №47
Установите соответствие между солью и типом ее гидролиза
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) KClO Б) KNO3 В) CsF |
1) гидролизуется и по катиону, и по аниону 2) гидролизу не подвергается 3) гидролизуется по катиону 4) гидролизуется по аниону |
Решение
Ответ: 424
Задание №48
Установите соответствие между солью и типом ее гидролиза
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) хлорид магния Б) нитрат аммония В) сульфит натрия |
1) гидролизуется по аниону 2) гидролизуется и по катиону, и по аниону 3) гидролизу не подвергается 4) гидролизуется по катиону |
Решение
Ответ: 441
Задание №49
Установите соответствие между солью и типом ее гидролиза
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) MnCl2 Б) CrCl3 В) NaI |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется и по катиону, и по аниону 4) гидролизу не подвергается |
Решение
Ответ: 114
Задание №50
Установите соответствие между солью и типом ее гидролиза
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) нитрат калия Б) бромид аммония В) хлорид рубидия |
1) гидролизу не подвергается 2) гидролизуется по катиону 3) гидролизуется по аниону 4) гидролизуется и по катиону, и по аниону |
Решение
Ответ: 121
[adsp-pro-3]
Задание №51
Установите соответствие между солью и ее отношением к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) CuS Б) K2CO3 В) CrCl3 |
1) гидролизуется и по катиону, и по аниону 2) гидролизу не подвергается 3) гидролизуется по катиону 4) гидролизуется по аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 243
Задание №52
Установите соответствие между солью и ее отношением к гидролизу
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) ацетат калия Б) фосфат натрия В) сульфат железа (III) |
1) гидролизуется по аниону 2) гидролизуется и по катиону, и по аниону 3) гидролизу не подвергается 4) гидролизуется по катиону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 114
Задание №53
Установите соответствие между солью и ее отношением к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) Ca(CH3COO)2 Б) Cu(NO3)2 В) NH4Br |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется и по катиону, и по аниону 4) гидролизу не подвергается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 211
Задание №54
Установите соответствие между солью и ее отношением к гидролизу
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) фторид цезия Б) гидрокарбонат кальция В) нитрат цинка |
1) гидролизу не подвергается 2) гидролизуется по катиону 3) гидролизуется по аниону 4) по катиону и аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 332
Задание №55
Установите соответствие между солью и ее отношением к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) KCl Б) NH4I В) BaBr2 |
1) по катиону и аниону 2) гидролизу не подвергается 3) гидролизуется по катиону 4) гидролизуется по аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 232
Задание №56
Установите соответствие между солью и ее отношением к гидролизу
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) гидрофосфат калия Б) нитрат меди В) ацетат цинка |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется и по катиону, и по аниону 4) гидролизу не подвергается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 213
Задание №57
Установите соответствие между солью и ее отношением к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) BeI2 Б) Cs2CO3 В) CuCl2 |
1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется и по катиону, и по аниону 4) гидролизу не подвергается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 121
Задание №58
Установите соответствие между солью и ее отношением к гидролизу
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) карбонат калия Б) силикат натрия В) иодид алюминия |
1) гидролизу не подвергается 2) гидролизуется по катиону 3) гидролизуется по аниону 4) по катиону и аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 332
Задание №59
Установите соответствие между солью и ее отношением к гидролизу
| ФОРМУЛА СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) Ba(NO3)2 Б) CaCl2 В) K3PO4 |
1) по катиону и аниону 2) гидролизу не подвергается 3) гидролизуется по катиону 4) гидролизуется по аниону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 224
Задание №60
Установите соответствие между солью и ее отношением к гидролизу
| НАЗВАНИЕ СОЛИ | ОТНОШЕНИЕ К ГИДРОЛИЗУ |
|
А) силикат калия Б) поташ В) аммиачная селитра |
1) гидролизуется по аниону 2) по катиону и аниону 3) гидролизу не подвергается 4) гидролизуется по катиону |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 114
[adsp-pro-3]
Задание №61
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) MgBr2 Б) BeCl2 В) K3PO4 |
1) красный 2) синий 3) оранжевый 4) фиолетовый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 112
Задание №62
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) хлорид калия Б) сульфат аммония В) ацетат натрия |
1) фиолетовый 2) красный 3) бесцветный 4) синий |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 124
Задание №63
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) MgCl2 Б) KNO3 В) NH4NO3 |
1) желтый 2) синий 3) фиолетовый 4) красный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 434
Задание №64
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) фторид калия Б) сульфат меди В) нитрат алюминия |
1) фиолетовый 2) красный 3) синий 4) черный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 322
Задание №65
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) Fe(NO3)3 Б) Rb2S В) ZnCl2 |
1) оранжевый 2) красный 3) фиолетовый 4) синий |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 242
Задание №66
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) бромид лития Б) карбонат цезия В) нитрат стронция |
1) красный 2) синий 3) зеленый 4) фиолетовый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 424
Задание №67
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) K3PO4 Б) KNO2 В) Cu(NO3)2 |
1) синий 2) красный 3) малиновый 4) фиолетовый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 112
Задание №68
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) хлорид магния Б) нитрат аммония В) гидросульфид натрия |
1) белый 2) фиолетовый 3) красный 4) синий |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 334
Задание №69
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) BeBr2 Б) ZnSO4 В) CuCl2 |
1) желтый 2) фиолетовый 3) синий 4) красный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 444
Задание №70
Установите соответствие между солью и изменением окраски лакмуса в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) нитрат калия Б) бромид аммония В) хлорид рубидия |
1) красный 2) оранжевый 3) фиолетовый 4) синий |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 313
[adsp-pro-3]
Задание №71
Установите соответствие между солью и изменением окраски фенолфталеина в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) BeBr2 Б) SnCl2 В) Rb2S |
1) бесцветный 2) черный 3) малиновый 4) синий |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 113
Задание №72
Установите соответствие между солью и изменением окраски фенолфталеина в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) ацетат калия Б) фосфат натрия В) сульфат железа (III) |
1) оранжевый 2) малиновый 3) фиолетовый 4) бесцветный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 224
Задание №73
Установите соответствие между солью и изменением окраски фенолфталеина в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) FeSO4 Б) Na2CO3 В) FeBr2 |
1) бесцветный 2) оранжевый 3) малиновый 4) желтый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 131
Задание №74
Установите соответствие между солью и изменением окраски фенолфталеина в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) фторид цезия Б) карбонат калия В) нитрат цинка |
1) малиновый 2) зеленый 3) бесцветный 4) голубой |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 113
Задание №75
Установите соответствие между солью и изменением окраски фенолфталеина в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) FeSO4 Б) K2SO4 В) CsCl |
1) коричневый 2) синий 3) малиновый 4) бесцветный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 444
Задание №76
Установите соответствие между солью и изменением окраски метилоранжа в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) гидрофосфат калия Б) нитрат меди В) ацетат калия |
1) красный 2) желтый 3) синий 4) черный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 212
Задание №77
Установите соответствие между солью и изменением окраски метилоранжа в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) CuSO4 Б) LiClO3 В) BaCl2 |
1) оранжевый 2) бесцветный 3) красный 4) желтый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 311 Решение
Задание №78
Установите соответствие между солью и изменением окраски метилоранжа в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) карбонат калия Б) силикат натрия В) иодид алюминия |
1) синий 2) оранжевый 3) желтый 4) красный |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 334
Задание №79
Установите соответствие между солью и изменением окраски метилоранжа в ее растворе
| ФОРМУЛА СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) Na2SiO3 Б) K2SO4 В) Rb2SO3 |
1) фиолетовый 2) красный 3) оранжевый 4) желтый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 434
Задание №80
Установите соответствие между солью и изменением окраски метилоранжа в ее растворе
| НАЗВАНИЕ СОЛИ | ЦВЕТ ИНДИКАТОРА |
|
А) нитрат свинца Б) хлорид олова (II) В) бромид стронция |
1) оранжевый 2) желтый 3) красный 4) фиолетовый |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Решение
Ответ: 331
[adsp-pro-3]
Задание №81
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
- 1. KCl
- 2. Fe(NO3)3
- 3. BaBr2
- 4. ZnCl2
- 5. NaI
Решение
Ответ: 24
Задание №82
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
1) карбонат калия
2) силикат натрия
3) иодид алюминия
4) хлорид кальция
5) нитрат марганца (II)
Решение
Ответ: 12
Задание №83
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
- 1. RbHS
- 2. Ca(NO3)2
- 3. FeSO4
- 4. BeSO4
- 5. SrCl2
Решение
Ответ: 25
Задание №84
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
1) силикат калия
2) поташ
3) аммиачная селитра
4) питьевая сода
5) медный купорос
Решение
Ответ: 35
Задание №85
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
- 1. Na2CO3
- 2. LiCl
- 3. KHСO3
- 4. FeI2
- 5. Al2(SO4)3
Решение
Ответ: 13
Задание №86
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
1) хлорид калия
2) сульфат аммония
3) ацетат лития
4) карбонат калия
5) гидрокарбонат натрия
Решение
Ответ: 1
Задание №87
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
- 1. HgCl2
- 2. CsI
- 3. NaF
- 4. CuSO4
- 5. Mg(NO3)2
Решение
Ответ: 145
Задание №88
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
1) фторид калия
2) сульфат меди
3) нитрат алюминия
4) гидросульфид натрия
5) гидрофосфат аммония
Решение
Ответ: 14
Задание №89
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
- 1. Ba(CH3COO)2
- 2. NaCl
- 3. BeSO4
- 4. AlBr3
- 5. Cr(NO3)3
Решение
Ответ: 2
Задание №90
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
1) бромид лития
2) карбонат цезия
3) нитрат стронция
4) нитрат цинка
5) фторид натрия
Решение
Ответ: 4
[adsp-pro-3]
Задание №91
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
- 1. NaHSO4
- 2. Fe2(SO4)3
- 3. CrCl3
- 4. Mn(NO3)2
- 5. RbNO2
Решение
Ответ: 5
Задание №92
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
1) хлорат калия
2) нитрат аммония
3) карбонат натрия
4) фосфат натрия
5) иодид лития
Решение
Ответ: 15
Задание №93
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
- 1. Ba(NO3)2
- 2. BeBr2
- 3. KClO3
- 4. CuCl2
- 5. ZnSO4
Решение
Ответ: 245
Задание №94
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
1) нитрат калия
2) бромид аммония
3) хлорид рубидия
4) сульфид цезия
5) нитрат стронция
Решение
Ответ: 4
Задание №95
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
- 1. Na2HPO4
- 2. CaSO4
- 3. CuCl2
- 4. Cs2SO4
- 5. KI
Решение
Ответ: 245
Задание №96
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
1) ацетат калия
2) фосфат натрия
3) сульфат железа (III)
4) сульфат железа (II)
5) нитрат хрома (III)
Решение
Ответ: 345
Задание №97
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
- 1. KMnO4
- 2. K2SO4
- 3. LiClO
- 4. KClO3
- 5. BeCl2
Решение
Ответ: 3
Задание №98
Какие из приведенных солей будут иметь нейтральную среду раствора. Число верных ответов может быть любым
1) гидрофосфат калия
2) нитрат меди
3) нитрат цинка
4) сульфат натрия
5) сульфат алюминия
Решение
Ответ: 4
Задание №99
Какие из приведенных солей будут иметь кислую среду раствора. Число верных ответов может быть любым
- 1. LiI
- 2. KClO
- 3. NaClO2
- 4. RbClO3
- 5. Zn(NO3)2
Решение
Ответ: 5
Задание №100
Какие из приведенных солей будут иметь щелочную среду раствора. Число верных ответов может быть любым
1) карбонат калия
2) силикат натрия
3) иодид алюминия
4) хлорид кальция
5) нитрат марганца (II)
Решение
Ответ: 12
[adsp-pro-10]
Гидролиз (греч. hydor — вода и lysis — разрушение) — процесс расщепления молекул сложных химических веществ за счет
реакции с молекулами воды.
В химии, как и в жизни, разрушается чаще всего нестойкое и слабое (стойкое и сильное выдерживает удар). Запомните, что гидролиз
(вода) разрушает «слабое» — это правило вам очень пригодится.

Любая соль состоит из остатка основания и кислоты. Абсолютно любая:
- NaCl — производное основания NaOH и кислоты HCl
- KNO3 — производное основания KOH и кислоты HNO3
- CuSO4 — производное основания Cu(OH)2 и кислоты H2SO4
- Al3PO4 — производное основания Al(OH)3 и кислоты H3PO4
- Ca(NO2)2 — производное основания Ca(OH)2 и кислоты HNO2
Чтобы успешно решать задания по теме гидролиза и писать реакции, вам следует запомнить, какие основания и кислоты являются
слабыми, а какие — сильными.
При изучении гидролиза я рекомендую ученикам сохранить на гаджет схему, которую вы видите ниже. Для того, чтобы приобрести
нужный опыт — она незаменима. Пользуйтесь ей как можно чаще, подглядывайте в нее и она незаметно окажется в вашем
интеллектуальном составляющем 

По катиону, по аниону или нет гидролиза?
Итак, если в состав соли входит остаток сильного основания и остаток сильной кислоты — гидролиза не происходит. Примеры: NaCl, KBr,
CaSO4. Также гидролиза не происходит, если соль нерастворима (вне зависимости от того, чем она образована): AlPO4,
FeSO3, CaSO3.
Если в состав соли входит остаток слабого основания и остаток сильной кислоты, то гидролиз идет по катиону. Помните, что гидролиз
разрушает слабое, в данном случае — катион. Примеры: AlCl3, MgBr2, Cr2SO4, NH4NO3.
Катион NH4+ и его основание NH4OH , несмотря на растворимость, является слабым, поэтому гидролиз будет идти
по катиону в соли NH4Cl. Замечу также, что Ca(OH)2 считается растворимым основанием, поэтому гидролиза соли CaCl2
не происходит.
Если в состав соли входит остаток сильного основания и остаток слабой кислоты, то гидролиз идет по аниону. Примеры: K3PO4,
NaNO2, Ca(OCl)2, Ba(CH3COO)2, K2SiO3.
Если соль образована остатком слабого основания и слабой кислоты, то гидролиз идет и по катиону, и по аниону. Примеры: Mg(NO2)2,
Al2S3, Cr2(SO3)3, CH3COONH4.
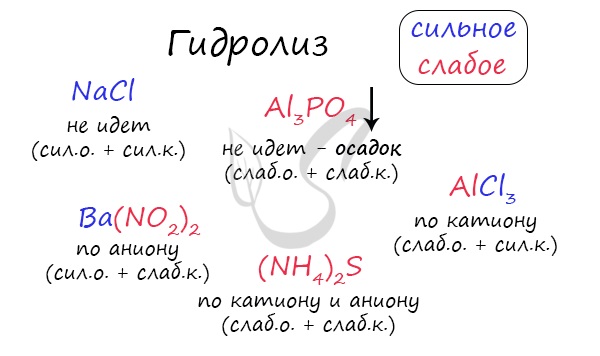
Самостоятельно определите тип гидролиза для CaI2, Li2SiO3, Ba(NO2)2, CuBr2, Zn(H2PO4)2.
Ниже вы найдете решение.
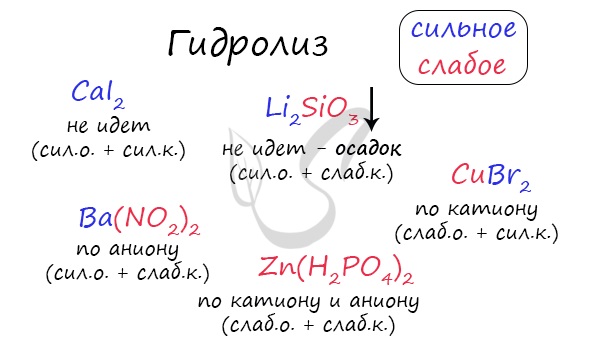
Среда раствора
Среда раствора может быть нейтральной, кислой или щелочной. Определяется типом гидролиза. Некоторые задания могут быть построены так, что, увидев соль,
вы должны будете определить ее тип раствора.
Обрадую вас: если вы усвоили тему гидролиза, сделать это проще простого. В случае, когда гидролиз не идет или идет и по катиону, и по аниону среда
раствора — нейтральная.
Если гидролиз идет по катиону (разрушается остаток основания) среда — кислая, если гидролиз идет по аниону (разрушается остаток кислоты), то среда
раствора будет щелочная. Изучите примеры.
Однако замечу, что в дигидрофосфатах, гидросульфитах и гидросульфатах среда всегда кислая из-за особенностей диссоциации. Примеры:
NH4H2PO4, LiHSO4. В гидрофосфатах среда щелочная из-за того, что константа диссоциации по третьей ступени меньше, чем константа гидролиза. Примеры: K2HPO4, Na2HPO4.

Попробуйте определить среду раствора для соединений из самостоятельного задания, которое вы только что решили.
Ниже будет располагаться решение.

С целью запутать в заданиях часто бывают даны синонимы. Так «среду раствора» могут заменить водородным показателем pH.
Запомните, что кислая среда характеризуется pH < 7. В нейтральной pH = 7. В щелочной pH > 7.
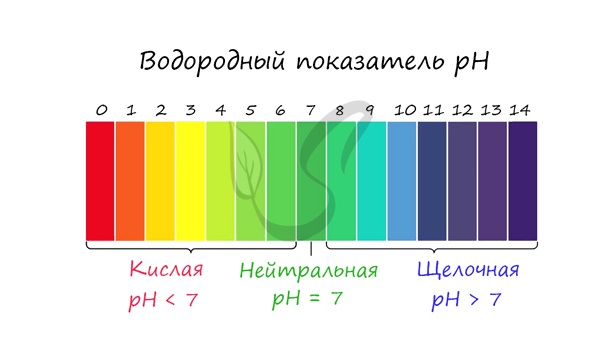
Например, в соли CaCl2 среда раствора будет нейтральной (pH=7), а в растворе AlCl3 — кислой (pH < 7).
Индикаторы (лат. indicator — указатель)
Индикатор — вещество, используемое в химии для определения среды раствора. В зависимости от среды раствора индикатор способен
менять его цвет, что наглядно отражает характер среды в определенный момент времени.
Наиболее известные и широко применяемые индикаторы: лакмус, фенолфталеиновый и метиловый оранжевый. В зависимости от среды
раствора их окраска меняется, что отражает приведенная ниже таблица.

Для тех, кто обладает хорошей зрительной памятью, будет несложно запомнить эту схему. Но что делать аудиалам и кинестетикам? 
От волнения на экзамене такая таблица легко может раствориться и перепутаться в океане мыслей, поэтому своим ученикам я рекомендую
запомнить индикаторы по стихам.
Только представьте, как приятно будет прочитать стих на экзамене, и убедиться в его безошибочности. Это придаст уверенности и поднимет
настроение 
Лакмус
Индикатор лакмус красный
Кислоту укажет ясно.
Индикатор лакмус синий —
Щелочь здесь, не будь разиней!
Когда ж нейтральная среда,
Он фиолетовый всегда.
Фенолфталеин
Фенолфталеиновый
В щелочах малиновый
Несмотря на это —
В кислотах он без цвета.
Метиловый оранжевый
От щелочи я желт как в лихорадке
Я розовею от кислот, как от стыда
И я бросаюсь в воду без оглядки —
Здесь я оранжевый практически всегда!

© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Гидролиз неорганических веществ
Ионообменной
реакции с водой – гидролизу, подвергаются многие неорганические и органические вещества.
Это приходится учитывать при хранении растворов, например, лекарств, или сухих
веществ во влажной атмосфере.
В случае взаимодействия аниона растворенной соли с водой процесс
называется гидролизом соли по аниону:
1) KNO2
D K+
+ NO2− (диссоциация)
2) NO2 ― + HOH « HNO2
+ OH− (гидролиз)
Диссоциация
соли KNO2 протекает полностью, а диссоциация азотистой кислоты HNO2
ничтожна, поэтому раствор стал щелочным (среди продуктов присутствует ион OH−).
Гидролизу подвергаются анионы только слабых кислот (в
данном примере − нитрит-ион NO2− , отвечающий слабой
азотистой кислоте HNO2). Анион слабой кислоты обладает способностью захватывать
катион водорода у молекулы воды, образуя молекулу соответствующей кислоты или
кислый анион и оставляя в растворе гидроксид-ион OH−.
Степень
протекания гидролиза увеличивается в ряду анионов:
F−, NO2−, CH3COO−,
SO32−, ClO−, CN−, CO32−,
PO43−, S2−, SiO32−
Примеры
реакций гидролиза анионов:
а) СO32−
+ HOH « HСO3−
+ OH−
б) PO43− + HOH « HPO42−
+ OH−
в) S2− + HOH « HS−
+ OH−
Ионы CO32−, PO43− и S2−
подвергаются гидролизу в большей степени, чем NO2−. Причина
этого состоит в том, что сила соответствующих кислот в указанном ряду
(азотистая − угольная по второй ступени − ортофосфорная по третьей ступени −
сероводородная по второй ступени) убывает. Поэтому растворы солей Na2CO3,
K3PO4 и BaS будут сильнощелочными
(рН > 7).
Соли, образованные катионом сильного основания и анионом слабой
кислоты, подвергаются гидролизу по аниону и создают в растворе щелочную среду.
Гидролиз солей по катиону
В случае взаимодействия катиона растворенной соли с водой процесс
называется гидролизом соли по катиону:
1) Ni(NO3)2
D Ni2+
+ 2NO3− (диссоциация)
2) Ni2+ + HOH « NiOH+
+ H+ (гидролиз)
Диссоциация
соли Ni(NO3)2 протекает полностью, а гидролиз катиона NiОН+
в очень малой степени, поэтому среда стала кислотной (среди продуктов присутствует
ион H+).
Гидролизу подвергаются катионы только малорастворимых основных и
амфотерных гидроксидов и катион аммония NH4+.
Катион металла, захватывая у молекулы воды гидроксил, освобождает катион
водорода H+ (катион оксония H3O+).
В результате
раствор становится кислотным
(избыток катионов оксония H3O+, рН < 7).
Катион аммония
в результате гидролиза образует слабое основание − гидрат аммиака и катион
водорода (катион оксония):
NH4+
+ H2O « NH3•H2O
+ H+
Степень
гидролиза катионов увеличивается в ряду
Ni2+, La3+, Mn2+, NH4+,
Co2+, Zn2+, Cd2+, Cu2+, Fe2+,
Pb2+, Al3+, Sc3+, Cr3+, Fe3+
Другие примеры:
а) Zn2+
+ H2O « ZnOH+
+ H+ (α = 0,05%)
б) Cr3+ + H2O « CrOH2+ + H+
(α = 3,3%)
в) Fe3+ + H2O « FeOH2+ + H+
(α = 22,8%)
Соли, образованные катионом малорастворимого основного или
амфотерного гидроксида и анионом сильной кислоты, подвергаются гидролизу по
катиону и образуют в растворе кислотную среду.
Гидролиз по катиону и аниону
Соли, образованные катионами малорастворимых основных или
амфотерных гидроксидов и анионами слабых кислот подвергаются полному гидролизу.
Например,
некоторые фториды и ацетаты этих металлов хорошо растворимы в воде; они
гидролизуются по катиону и аниону (в разной степени). Среда раствора
определяется тем ионом соли, у которого степень гидролиза выше (в большинстве
случаев выше степень гидролиза катионов и среда раствора слабокислотная).
Например,
гидролиз фторида меди(+2) протекает по схеме:
CuF2
D Cu2+
+ 2F−
Cu2+
+ HOН « CuOH+
+ H+ (α = 0,068%)
F− + HOН « HF + OH− (α = 0,0012%)
Преобладает кислотная
среда, так как степень гидролиза по катиону выше.
То же
наблюдается в растворах солей аммония − фторида аммония NH4F (среда
кислотная), ацетата аммония NH4CH3COO (среда практически
нейтральная из-за одинаковой степени гидролиза по катиону и по аниону) и
цианида аммония NH4CN (среда щелочная).
Многие
соединения, синтезируемые «сухим» способом − например карбонат железа(II),
сульфид алюминия − при попытке получения обменной реакцией в водном растворе
подвергаются полному необратимому гидролизу с образованием основных солей или
гидроксидов, а также соответствующих кислот или кислотных оксидов:
а) 2Fe2+
+ 2CO32− + HOН « Fe2CO3(OH)2↓
+ CO2↑
б) 2Al3+
+ 3S2− + 6HOН « 2Al(OH)3↓ + 3H2S↑
Гидролиз бинарных соединений
Многие
вещества, относящиеся к классу бинарных соединений и не являющиеся солями, не
могут существовать в водном растворе, поскольку подвергаются
полному необратимому гидролизу:
Mg3N2 + 8HOН « 3Mg(OH)2
+ 2NH3 • H2O
CaC2 + 2HOН « Ca(OH)2
+ C2H2
Поскольку гидролиз бинарных соединений протекает необратимо, следует оберегать
их от контакта с водой и влажным воздухом.
Гидролиз в заданиях ЕГЭ по химии
w Фенолфталеин можно использовать для обнаружения в водном
растворе соли
1) ацетата
алюминия
2) нитрата калия
3) сульфата алюминия
4) карбоната натрия
Фенолфталеин
– индикатор на щелочную среду, в которой он принимает малиновую окраску. В
растворе соли щелочная среда может возникнуть при гидролизе по аниону.
Анализируем:
1) ацетат
алюминия, полный гидролиз, среда слабокислая;
2) нитрат калия, кислота и основание сильные, гидролиз не идет, среда
нейтральная;
3) сульфат алюминия, сильная кислота и слабое основание, гидролиз по катиону,
среда кислая;
4) карбонат натрия ― соль, образованная слабой кислотой и сильным основанием:
гидролиз по аниону, среда щелочная:
Na2СO3+
HOH D HСO3–
+ OH – + 2Na+
Ответ: 4
w Среда
раствора силиката калия
1)
щелочная
2) кислая 3) нейтральная 4) слабокислая
w Установите соответствие между формулой соли и ионным уравнением
гидролиза этой соли:
|
ФОРМУЛА СОЛИ |
ИОННОЕ УРАВНЕНИЕ |
Ответ: 1В, 2Г,
3А, 4Б
w Как скажется на состоянии химического равновесия в системе?
Fe2+ + H2O D FeOH+ + H+ –
Q
1)
добавление H2SO4
2) добавление KOH
3) нагревание раствора
При ответе на этот вопрос надо учитывать, что добавляемые вещества –
электролиты. Поставляемые ими ионы могут, как непосредственно влиять на
равновесие, так и взаимодействовать с одним из ионов, участвующих в обратимой
реакции.
добавление H2SO4:
H2SO4 D 2H+
+ SO42–
повышение концентрации ионов водорода приводит, по принципу Ле Шателье, к
смещению равновесия в системе влево (обратная реакция)
добавление KOH:
KOHD K+
+ OH– ;
H+ + OH– «H2O
гидроксид-ионы связывают ионы водорода в малодиссоциирующее вещество, воду.
Снижение концентрации ионов водорода приводит, по принципу Ле Шателье, к
смещению равновесия в системе вправо (прямая реакция)
нагревание раствора
По принципу Ле Шателье, повышение температуры
приводит к смещению равновесия в сторону протекания эндотермической реакции,
т.е. – вправо (прямая реакция)
w Между собой водные растворы сульфата и фосфата натрия можно
различить с помощью
1) гидроксида
натрия
2) серной кислоты
3) фенолфталеина (так как Na3PO4 это
соль сильного основания и средне-слабой кислоты, гидролизуется по аниону)
4) фосфорной кислоты
w Установите
соответствие между названиями солей и средой их растворов.
|
НАЗВАНИЕ СОЛИ 1) |
СРЕДА А) |
Ответы:
1Б,
2А, 3В, 4А
w Установите соответствие между формулой соли и способностью этой
соли к гидролизу.
|
ФОРМУЛА СОЛИ 1) Zn(CH3COO)2 |
СПОСОБНОСТЬ А) |
Ответы:
1В,
2Г, 3Б, 4А


